Introduction
* our project is to make a "bacterial timer" i.e. ~~(もっとぐたいてきに).
- our approach to this goal is to make a series of a transcription factor which each of them differes in a responce time of the transcription activation by an same inducer.
- we believe that this device would be useful for making an macroscopic timing control in bacterial behavior or many application in synthetic biology & iGEM community.
- to demonstrate this "timing control", we aimed to draw an "animated picture": a picture that pop up one by one.
|
|
(手術予定)
- 細胞通信を使ったBacterial Timer を創ります。
- E. coli Timer完成予想図
- Timerを創る方法は様々(diffusion of molecules, switching(oscillator, communication, arabinose, plac, etc... ))であるが、なぜ細胞通信を選んだのか。
そして、昨年は2段階の通信しか創れなかった。バリエーションが乏しい。
- 作戦変更!(Sender側をかえたCrosstalk通信にはバリエーションを創るのに限界があるので、今年はReceiver側の調節をする。)目指すは時計の数字分の、12通りの時間差をつくりたい!
-
It has been demanded in biological engineering that making the function that organisms sense the passage of time. We can utilize the excellent functions of organisms such as material synthesis or sensing as a device for drug delivery system or physical exam when these functions have been time-controlled as we like. However we can control cells individually, without method to control them all together, advantage of excellent functions may attenuate. Then we want to make the timer that cells works concurrently.
Project Design
(手術予定)
2) Project Design
⑤Receiver側のAHL通信の仕組みを図説する。(1,AHLが入るところ(培地調節) 2,Receiver中のLuxR 3,Receiver中のReporter)
Team:Chiba/Project/Signaling-system
Experiments, Results & Discussion
- directed evolutionで色々な応答速度のLuxR mutantをつくることを目指した。
Experiments
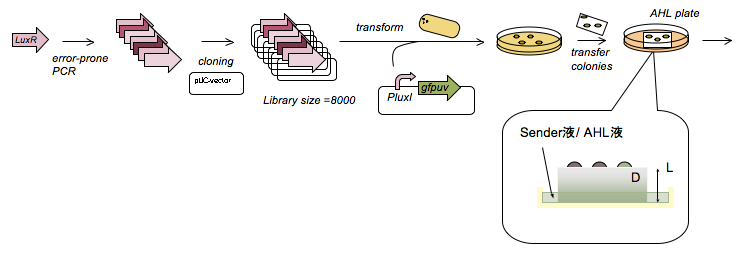 Fig. Y Directed evolution to get some delayed-LuxR mutants - error-prone PCRでLuxRの変異ライブラリを作製し,発現ベクターに組み込んだ
- これを,E.coli BW(?) harboring plux-gfpに形質転換し,コロニーを形成させた。
- コロニーをニトロセルロース膜でリフトし,AHL入りのプレートにのせ,gfpの蛍光の経時変化をみた(Fig. X)。
- 蛍光しはじめるのが遅いものを13個pickし,delayed-LuxR変異体を得た。
- pickした13個のクローンの転写活性化速度?を,再度transformして確認し,最終的に○個の速度バリエーションのluxR変異体を得た。
 Fig. X LuxRライブラリ?によるのPlux-gfp蛍光経時変化
(手術予定)
⑥Mutantを創る。(Error-proneが良い理由:バリエーションを創りやすい。新たなBiobrick作成方法としてError-prone PCRとスクリーニングをセットにしMutant-Partsの作り方を説明する。)
⑦さらに詳しい実験方法(Biobrickからerror-prone PCRをおこなったことなど)
⑧得られたデーター(なぜ8000のライブラリを、200に絞り、どうやって13sampleを選び出したのか説明)
得られたLuxR mutantのcharacterization
- この辺のデータ載せておいてください,明日みます!--Maiko 14:37, 20 October 2009 (UTC)
⑨LuxR Mutant 個性確定実験の実験方法
Team:Chiba/Project/characterization
まず、LuxR Mutantsとpositive controlとしてLuxR WT, negative control としてレポーターが含まれない菌をそれぞれグリストからつつき、12h@37℃液体培養。
・pC1A3-LuxR Mutants / pLux-GFP @JW1262 : Sample No.1~11, L1, L2
・pC1A3-LuxR WT / pLux-GFP @JW1262 : Positive control
・GFP等のレポーターが入っていない菌 : Negative control
次にCultureを48ピンでNCフィルタへ植菌し、フィルタを固体培地にのせて12h@37℃で培養。
最後にAHLの濃度を0, 1, 10, 100, 1000 nMで(一番最初の9月22日の実験は0, 10, 1000 nMでおこないました。)ふった固体培地に、NCフィルタを移動。
この時を測定開始点とし、30分毎に4時間蛍光の上がり方を目視で確認。
⑩100 nM培地での応答の遅れについての結果
⑪AHL濃度を振った場合の、6h後の蛍光強度の差についての結果
⑫LuxR Mutantの個性と、変位が入っている部分からの考察
To draw more better picture
- we screened the "agar media condition" (the thickness & the agar conc.) to make difference in the delay of the LuxR mutant more bigger(appearent?).
- ちょっと思ったのだがこのAHL濃度とか培地とかふりまくってるのを載せると,LuxRの時間差が見えた理由が「LuxR変異体のおかげ」というよりは「培地のおかげ」っぽくなるので,この培地スクリーニングは実は載せない(というかちっちゃくのせとくのは良いけどVIP待遇はしない)方がまだ恰好がつくのでは...^w^;--Maiko 14:05, 20 October 2009 (UTC)
- ”より差をみせるため”の実験なのでここでは軽く説明し、あとはリンクつけます。--Yoshimi 14:15, 20 October 2009 (UTC)
- そもそも「培地ふった実験」は項目なくても良いかも:デモらへんの実験条件にリンクつけるとか。レポーターは載せてもいいのでは(RFPはビミョーに差でたよね確か)--Maiko 14:34, 20 October 2009 (UTC)
ここに結果の写真だけのせる。--Yoshimi 14:17, 20 October 2009 (UTC)
培地のよりよい条件を見つける
私たちはデモをよりはっきり見せるために必要な培地の条件を調べた。
Team:Chiba/Project/medium
- ⑭Reporter毎の応答の差についての実験と結果。GFPuvがDelayを見やすい。
私たちは、ReporterとしてGFPuv, sfGFP, mRFP, mCherry, mOrangeを使って上に挙げたものと同じ実験をした。
その結果、GFPuvをReporterとして使った場合が最もmutant LuxR間の光り始める時刻の差をはっきりと確認できた。
最もmutant LuxR間の光り始める時刻の差を確認しやすかった条件は、以下の通りであった。
Reporter : GFPuv
medium : agar 5%
thickness : 7 mm
この条件でデモをやれば、各mutant LuxRの個性(遅れ方の特徴)を最大限に活かすことができると考えた。
そうするとメリハリのあるきれいなアニメーションを描くことが出来るのではないか。
Demonstration
⑯E. coli Timer完成デモ
明日の昼にはあげられます。--Yoshimi 14:21, 20 October 2009 (UTC)
(⑰できればアニメ)
Conclusions
手術予定
18・Biobrickを使って(iGEM的には)新たな方法(error-prone PCR)を用い、新パーツをつくりました。
- error-proneを用いて新パーツを作ったことではなく,そのスクリーニング法(AHL濃度が徐々に大きくなっていくとき,遅れて光る変異体をpick)が新しいと主張していたのではないでしょうか。--Masahiro 15:24, 20 October 2009 (UTC)
・何通り(ただいま確認中)のバリエーションの遅れを生み出せました。(Mutant+WT:4~5種、gel調節:2種、Reporters: 4通り・・・これらの組み合わせの分(タイミングがかぶるのは除く)だけ時間差をうみだせた!)
- LuxR以外の時間差は出さない方が良いです:転写だとかフォールディングだとかマチュレーションで時間差でるなら何故luxR変異体つくったのだという話になる:transcription activatorで差が出せたことをいうべし(ていうかそれが目的なのであり,何でもかんでも時間差が出したいというわけじゃない,よね,たしか)--Maiko 14:47, 20 October 2009 (UTC)
- 何でもかんでも時間差が出したい,という結論だったと思います(先日の梅ミーティングでは)。--Masahiro 15:30, 20 October 2009 (UTC)
・demonstrationをおこないました。
⑲ Future Works : Whisper down the lane
|
|
時計というものに、時間だけでなく順番も入れられる。
例えば培地中に拡散するAHLにムラがあったとしても、ちゃんと順番通りに動くシステム、
バリエーションは作れないが順番ならば得意。
成長するアニメーションを作るには、この順番通りに動くシステムが必要。
アニメを作るときは時間の刻み方が人にとって意味を持つようなものであることが大切。
|
|  "
"

