Team:SupBiotech-Paris/Thérapies actuelles
From 2009.igem.org
Contents |
Les thérapies actuelles [1]
Les médicaments actuels
Les médicaments sont des entités chimiques ou biologiques, qui contiennent au moins un principe actif, et agissent sur une cible cellulaire, en vue d’un intérêt thérapeutique.
Dans le langage courant un médicament est une substance administrée pour corriger, modifier ou restaurer une fonction affectée de l’organisme.
D’un point de vue chimique, un médicament est une molécule (parfois un élément (ions)) qui interagit avec une cible moléculaire, c’est-à-dire avec un récepteur biologique. La liaison du médicament modifie alors les propriétés de la cible, ce qui conduit à une réponse de la cellule. Ceci est à l’origine des effets bénéfiques et indésirables d’un médicament.
La plupart des médicaments actuels ont une cible protéique. Les protéines sont indispensables à la survie de notre organisme. La majorité des maladies humaines sont associées à leur disfonctionnement. De nos jours, un bon nombre de protéines peuvent être facilement produites grâce à l’ingénierie génétique, elles peuvent ainsi être utilisées comme un traitement efficace pour un large spectre de maladies, dues à des protéines absentes ou déficientes.
Pour le traitement contre le cancer, les médicaments agissent comme des inhibiteurs de la mitose. La sélectivité toxique des cytotoxiques est liée pour l'essentiel à l'intense activité mitotique des cellules cancéreuses qui fait de celles-ci une cible statistiquement préférentielle. La sélectivité est une notion importante à la connaissance du médicament. En effet, aucun médicament n’est réellement spécifique. Ainsi les tissus normaux à renouvellement cellulaire rapide sont eux aussi, fréquemment lésés : épithéliums, phanères, moelle osseuse, et gonades.
Il est indispensable de bien caractériser un médicament. On étudie alors plusieurs paramètres comme la biodisponibilité et la vitesse de résorption du médicament. La biodisponibilité d’un médicament peut être incomplète à cause de différents phénomènes comme les caractéristiques physico-chimiques des médicaments ou l’effet du premier passage intestinal, hépatique ou pulmonaire.
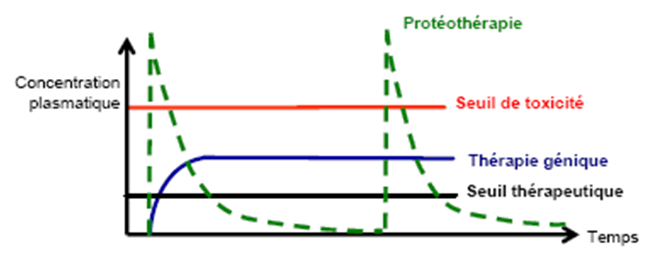
La vitesse à laquelle le médicament est résorbé est également un paramètre important pour toutes les voies d’administration autres que la voie intra-veineuse. Le délai avant l’observation des premiers effets (thérapeutiques ou indésirables) du médicament dépend aussi de cette vitesse. De plus, l’existence d’un rythme biologique est souvent négligée lors de l’évaluation de leur résorption. Pourtant, les propriétés pharmacologiques des médicaments sont étroitement liées au phénomène de temporalité du médicament. Plusieurs notions complémentaires et importantes doivent être envisagées : celle de vitesse de résorption, et de seuil de toxicité.
Les problèmes majeurs que rencontrent ces thérapies sont les variabilités inter-patients dans les réactions aux médicaments qui deviennent une difficulté conséquente à la fois au niveau de la recherche pharmaceutique et au niveau médical.
Dans cette optique, pour améliorer l’efficacité des thérapies, une nouvelle pharmacologie ayant l’ADN génomique ou les ARN pour cibles, a été développée : la pharmacologie génétique.
L’intérêt de la pharmacologie génétique [1,2]
Le défi de la thérapie génique est de parvenir à corriger, à l'intérieur des cellules d'un organisme humain (via des modifications sur le génome), les anomalies qui engendrent une maladie. Contrairement à la thérapie protéique, la thérapie génique ne se contente pas d’atténuer les symptômes mais va bien plus loin : son objectif est leur suppression.
Même lorsqu’une protéine exogène peut être utilisée, la thérapie génique présente des avantages majeurs :
- La protéine produite à partir du transgène est soumise aux processus de modifications post-transcriptionnels de l’hôte. Le profil de glycosylation est donc strictement celui du patient, ce qui assure ainsi une meilleure biocompatibilité.
- Elle permet de contourner le problème de l’administration de protéines complexes à l’intérieur de la cellule, étant donné que le transgène est exprimé directement à travers la machinerie cellulaire.
- Elle permet une expression localisée du transgène, évitant tout risque lié à la présence systémique de la protéine.
La thérapie génique a l’avantage de présenter une meilleure pharmacocinétique en évitant les administrations répétées du traitement et la toxicité qui leur est liée. Elle permet également une expression prolongée du gène-médicament puisque l’activité biologique des protéines transgéniques semble être supérieure à celle des protéines recombinantes. De plus, la suppression des pics d’injection permet d’éviter une désensibilisation des récepteurs.
Pour finir, un dernier point, qui peut paraitre moins crucial, mais qui a néanmoins son importance : le confort du malade. L’administration unique (ou répétée à très faible fréquence) est beaucoup mieux tolérée par le malade qu’une administration quotidienne, voir pluriquotidienne, comme c’est le cas actuellement pour l’insuline dans le traitement du diabète. D’ailleurs, l’aspect financier n’est pas négligeable, puisque l’administration des médicaments chimiques ou biologiques s’effectue en ambulatoire ou à l’hôpital et, ainsi, handicape encore leur généralisation. De même, le coût d’une extraction et d’une purification de protéine recombinante est bien supérieur à la synthèse d’un oligonucléotide.
Conclusion
L’instabilité des protéines, leurs difficultés à être produites, et également leur déficience intracellulaire, sont responsables d’un grand nombre de maladies. Cela met ainsi en évidence l’intérêt que suscite le gène médicament.
Peu de traitements ont réellement prouvé leur efficacité, sans apporter une forte toxicité. Pour cette raison, la thérapie génique apparait comme une approche fort prometteuse. Transformer le gène en médicament apparaît ainsi comme une stratégie séduisante.
 "
"