Team:SupBiotech-Paris/Concept2Fr
From 2009.igem.org
Enguerrand (Talk | contribs) (→L’encapsidation du plasmide thérapeutique) |
Enguerrand (Talk | contribs) (→La délivrance du vecteur cellulaire dans l’organe cible [1,2,8]) |
||
| (63 intermediate revisions not shown) | |||
| Line 8: | Line 8: | ||
<br> | <br> | ||
Vous allez pouvoir découvrir au cours de ce chapitre sur quelles caractéristiques nous nous sommes basés pour choisir le '''meilleur bactériophage'''.<br> | Vous allez pouvoir découvrir au cours de ce chapitre sur quelles caractéristiques nous nous sommes basés pour choisir le '''meilleur bactériophage'''.<br> | ||
| - | Puis, vous découvrirez plus en détails ses propriétés au travers des différentes contraintes imposées par le DVS concernant sa [[Team:SupBiotech-Paris/ | + | Puis, vous découvrirez plus en détails ses propriétés au travers des différentes contraintes imposées par le [[Team:SupBiotech-Paris/Introduction1Fr#DVS|DVS]] concernant sa '''[[Team:SupBiotech-Paris/Concept1Fr#DT|délivrance tissulaire]]''', '''l’encapsidation du [[Team:SupBiotech-Paris/Concept3Fr#drapeau|plasmide thérapeutique]]''' et le '''ciblage cellulaire'''.<br> |
| + | |||
<span style="float: right">[[Team:SupBiotech-Paris/Concept2Fr#drapeau|Haut de page]]</span> | <span style="float: right">[[Team:SupBiotech-Paris/Concept2Fr#drapeau|Haut de page]]</span> | ||
| - | == Le vecteur cellulaire : Le bactériophage Lambda == | + | == Le vecteur cellulaire : Le bactériophage Lambda [1,2] == |
| + | |||
| + | Nous avons étudié plusieurs types de bactériophages afin de sélectionner le vecteur cellulaire le plus modulable et le plus contrôlable. Pour se faire, nous avons répertorié tous les types de phages et au sein de chaque type, les espèces les mieux décrites. Plusieurs candidats ont retenu notre attention, mais c’est le bactériophage lambda qui nous a semblé le plus adapté.<br> | ||
| + | |||
| + | Le bactériophage lambda est un virus procaryote qui infecte naturellement la bactérie Escherichia Coli. C’est un bactériophage dit tempéré, car il peut alterner phase lytique et phase lysogène sous certaines conditions. Pendant le cycle lytique, l’ADN circulaire est répliqué en grande quantité dans le cytoplasme, des progénies viraux sont formés, conduisant à la mort de la bactérie et à la libération des virions. Au cours du cycle lysogène, le génome du bactériophage est intégré dans le chromosome bactérien et est transmis à la descendance. La réplication se fait alors au rythme des divisions de la bactérie.<br> | ||
| - | |||
| - | |||
| - | |||
| - | |||
Naturellement infectieux pour la bactérie Escherichia Coli, le bactériophage lambda, comme tous phages, n’est pas infectieux pour l’Homme. Cette caractéristique provient du fait que leur génome est régie par des promoteurs procaryotes mais également du fait qu’ils aient une très faible capacité de transfection des cellules eucaryotes. <br> | Naturellement infectieux pour la bactérie Escherichia Coli, le bactériophage lambda, comme tous phages, n’est pas infectieux pour l’Homme. Cette caractéristique provient du fait que leur génome est régie par des promoteurs procaryotes mais également du fait qu’ils aient une très faible capacité de transfection des cellules eucaryotes. <br> | ||
Enfin, l’une des caractéristiques intéressantes du bactériophage lambda est qu’il possède un ADN double brin linéaire ayant des extrémités cohésives : 12 nucléotides simple brin complémentaire, appelés séquences « Cos ». Ces extrémités cohésives ont une fonction dans '''l’encapsidation génomique'''.<br> | Enfin, l’une des caractéristiques intéressantes du bactériophage lambda est qu’il possède un ADN double brin linéaire ayant des extrémités cohésives : 12 nucléotides simple brin complémentaire, appelés séquences « Cos ». Ces extrémités cohésives ont une fonction dans '''l’encapsidation génomique'''.<br> | ||
| + | |||
<span style="float: right">[[Team:SupBiotech-Paris/Concept2Fr#drapeau|Haut de page]]</span> | <span style="float: right">[[Team:SupBiotech-Paris/Concept2Fr#drapeau|Haut de page]]</span> | ||
| - | == L’encapsidation du plasmide thérapeutique == | + | == L’encapsidation du plasmide thérapeutique [2,3,4,5,6,7] == |
| - | L’encapsidation du génome phagique est particulière chez le bactériophage lambda. Elle est guidée par la | + | L’encapsidation du génome phagique est particulière chez le bactériophage lambda. Elle est guidée par la [[Team:SupBiotech-Paris/Concept3Fr#cos|séquence Cos]]. Cette caractéristique permet l’encapsidation spécifique de séquence d’intérêt.<br> |
| - | [[Image :Encapsidation.png|center|frameless]] | + | |
| - | + | ||
| - | On observe sur le schéma ci-dessus que l’encapsidation du génome commence et se termine par les | + | [[Image:Encapsidation.png|center|650px|frameless]] |
| - | Nous sommes partis de ce constat pour encapsider, à l’intérieur du vecteur cellulaire, uniquement le [[Team:SupBiotech-Paris/Concept3Fr#drapeau|plasmide thérapeutique]]. Pour se faire le génome du vecteur, le bactériophage lambda, est délété de ses | + | |
| + | |||
| + | On observe sur le schéma ci-dessus que l’encapsidation du génome commence et se termine par les [[Team:SupBiotech-Paris/Concept3Fr#cos|séquences Cos]]. Tout ce qui se trouve entre ces séquences est encapsidé. Cette particularité est utilisée en biologie moléculaire depuis de nombreuses années pour la création de banque d’ADN et d’outils moléculaires nommés Cosmides.<br> | ||
| + | Nous sommes partis de ce constat pour encapsider, à l’intérieur du vecteur cellulaire, uniquement le [[Team:SupBiotech-Paris/Concept3Fr#drapeau|plasmide thérapeutique]]. Pour se faire le génome du vecteur, le bactériophage lambda, est délété de ses [[Team:SupBiotech-Paris/Concept3Fr#cos|séquences Cos]], ces dernières sont placées sur le [[Team:SupBiotech-Paris/Concept3Fr#drapeau|plasmide thérapeutique]].<br> | ||
| - | Séquence non codante cos : Position 1-132 et 48462-48502 : 174 paires de bases. | + | Séquence non codante cos : Position 1-132 et 48462-48502 : 174 paires de bases.<br> |
1.....TATCACTTTACGGGTCCTTTCCGGTGATCCGACAGGTTAC<br> | 1.....TATCACTTTACGGGTCCTTTCCGGTGATCCGACAGGTTAC<br> | ||
41....GGGGCGGCGACCTCGCGGGTTTTCGCTATTTATGAAAATT<br> | 41....GGGGCGGCGACCTCGCGGGTTTTCGCTATTTATGAAAATT<br> | ||
| Line 38: | Line 43: | ||
161...GACAGGTGCTGAA<br> | 161...GACAGGTGCTGAA<br> | ||
| - | |||
| - | |||
| - | Le vecteur cellulaire encapside le plasmide thérapeutique par l’intermédiaire des | + | Le vecteur cellulaire encapside le plasmide thérapeutique par l’intermédiaire des [[Team:SupBiotech-Paris/Concept3Fr#cos|séquences Cos]]. Ainsi, il ne délivre que l’[[Team:SupBiotech-Paris/Concept3Fr#drapeau|agent thérapeutique]] dans les cellules, ce qui permet une précaution supplémentaire au cas où le vecteur d’intérêt ne serait pas dans l’organe cible.<br> |
| + | |||
<span style="float: right">[[Team:SupBiotech-Paris/Concept2Fr#drapeau|Haut de page]]</span> | <span style="float: right">[[Team:SupBiotech-Paris/Concept2Fr#drapeau|Haut de page]]</span> | ||
| - | == La délivrance du vecteur cellulaire dans l’organe cible == | + | <div id="C1"></div> |
| + | |||
| + | == La délivrance du vecteur cellulaire dans l’organe cible [1,2,8]== | ||
| - | Le vecteur cellulaire possède deux phases d’action, une phase de '''latence''' et une phase d’'''expression et de libération'''. Lors de la phase de latence, appelée '''cycle lysogène''', le génome reste « inactif » et aucun vecteur cellulaire n’est produit au sein du vecteur tissulaire. Alors que pendant la phase d’expression et de libération, appelée '''cycle lytique''', le génome est transcrit et répliqué, afin de produire des vecteurs cellulaires.<br> | + | Le vecteur cellulaire possède deux phases d’action, une phase de '''latence''' et une phase d’'''expression et de libération'''. Lors de la phase de latence, appelée '''cycle lysogène''', le génome reste « inactif » et aucun vecteur cellulaire n’est produit au sein du [[Team:SupBiotech-Paris/Concept1Fr#drapeau|vecteur tissulaire]]. Alors que pendant la phase d’expression et de libération, appelée '''cycle lytique''', le génome est transcrit et répliqué, afin de produire des vecteurs cellulaires.<br> |
| - | Cependant le vecteur tissulaire n’est pas l’hôte naturelle du vecteur cellulaire. Ainsi, si l’on veut induire une phase de latence, il nous faut la provoquer. Le système de délivrance implanté dans le vecteur tissulaire induit justement cette phase de latence.<br> | + | Cependant le vecteur tissulaire n’est pas l’hôte naturelle du vecteur cellulaire. Ainsi, si l’on veut induire une phase de latence, il nous faut la provoquer. Le système de délivrance implanté dans le [[Team:SupBiotech-Paris/Concept1Fr#drapeau|vecteur tissulaire]] induit justement cette phase de latence.<br> |
Le plasmide de contrôle de délivrance du vecteur cellulaire induit un cycle lysogène chez ce dernier. <br> | Le plasmide de contrôle de délivrance du vecteur cellulaire induit un cycle lysogène chez ce dernier. <br> | ||
Le cycle lysogène est un phénomène naturellement présent chez le bactériophage lambda, le vecteur cellulaire. Lors de ce cycle, le génome phagique est inséré dans le génome bactérien sous la forme d’un prophage, il devient partie intégrante du génome de l’hôte.<br> | Le cycle lysogène est un phénomène naturellement présent chez le bactériophage lambda, le vecteur cellulaire. Lors de ce cycle, le génome phagique est inséré dans le génome bactérien sous la forme d’un prophage, il devient partie intégrante du génome de l’hôte.<br> | ||
A l’état de prophage, toute transcription est réprimée. Seul le gène cI, responsable du maintien du cycle lysogène, est exprimé.<br> | A l’état de prophage, toute transcription est réprimée. Seul le gène cI, responsable du maintien du cycle lysogène, est exprimé.<br> | ||
| - | + | ||
| + | <html> | ||
| + | <center> | ||
| + | <embed | ||
| + | src="https://static.igem.org/mediawiki/2009/9/91/RepressionCI.swf" | ||
| + | width="650" | ||
| + | height="200" | ||
| + | allowscriptaccess="always" | ||
| + | allowfullscreen="true" | ||
| + | /> | ||
| + | </center> | ||
| + | </html> | ||
La fixation de cI sur les opérateurs de la région de contrôle des promoteurs pR et pL, bloque l’expression des gènes et permet le maintien de la lysogénie. cI bloque de surcroit son propre promoteur, pRM, permettant ainsi une autorégulation de sa transcription.<br> | La fixation de cI sur les opérateurs de la région de contrôle des promoteurs pR et pL, bloque l’expression des gènes et permet le maintien de la lysogénie. cI bloque de surcroit son propre promoteur, pRM, permettant ainsi une autorégulation de sa transcription.<br> | ||
| - | Le bactériophage est maintenu sous la forme lysogène aussi longtemps que cI est exprimé. Dans le cas du [[Team:SupBiotech-Paris/Introduction1Fr# | + | Le bactériophage est maintenu sous la forme lysogène aussi longtemps que cI est exprimé. Dans le cas du [[Team:SupBiotech-Paris/Introduction1Fr#DVS|DVS]], l’expression de cI n’est plus contrôlée par le promoteur pRM, mais induite par un [[Team:SupBiotech-Paris/BiobricksFr#drapeau|promoteur répressible LacP/O]] fusionné au gène cI. Si celui-ci n’est pas répressé, alors, comme dans le schéma naturel du bactériophage lambda, l’expression des gènes est inhibée.<br> |
| - | + | ||
| - | + | ||
| - | + | ||
En revanche, lorsque le signal de délivrance du vecteur cellulaire, la doxycycline, est injecté, alors le [[Team:SupBiotech-Paris/BiobricksFr#drapeau|promoteur répressible LacP/O]] est réprimé par le répresseur LacI, synthétisé par le [[Team:SupBiotech-Paris/Concept1Fr#drapeau|vecteur tissulaire]]. | En revanche, lorsque le signal de délivrance du vecteur cellulaire, la doxycycline, est injecté, alors le [[Team:SupBiotech-Paris/BiobricksFr#drapeau|promoteur répressible LacP/O]] est réprimé par le répresseur LacI, synthétisé par le [[Team:SupBiotech-Paris/Concept1Fr#drapeau|vecteur tissulaire]]. | ||
cI inhibé, les gènes peuvent alors être transcrits, et le vecteur cellulaire synthétisé. <br> | cI inhibé, les gènes peuvent alors être transcrits, et le vecteur cellulaire synthétisé. <br> | ||
| - | Système sans doxycycline: <br> | + | <u>Système sans doxycycline:<br></u> |
| - | + | <html> | |
| - | + | <center> | |
| - | Système avec doxycycline: <br> | + | <embed |
| - | + | src="https://static.igem.org/mediawiki/2009/1/14/Nodoxy.swf" | |
| + | width="650" | ||
| + | height="200" | ||
| + | allowscriptaccess="always" | ||
| + | allowfullscreen="true" | ||
| + | /> | ||
| + | </center> | ||
| + | </html> | ||
| + | <html> | ||
| + | <div style="float: left; margin-left: -150px;"> | ||
| + | <img title="Le système de contrôle de lyse" style="width: 150px;" src="https://static.igem.org/mediawiki/2009/2/2f/Bibou4.png";> | ||
| + | </div> | ||
| + | </html> | ||
| + | <u>Système avec doxycycline: <br></u> | ||
| + | <html> | ||
| + | <center> | ||
| + | <embed | ||
| + | src="https://static.igem.org/mediawiki/2009/7/7d/Avecdoxy.swf" | ||
| + | width="650" | ||
| + | height="200" | ||
| + | allowscriptaccess="always" | ||
| + | allowfullscreen="true" | ||
| + | /> | ||
| + | </center> | ||
| + | </html> | ||
| - | Lors de sa libération le vecteur cellulaire lyse le [[Team:SupBiotech-Paris/Concept1Fr#drapeau|vecteur tissulaire]]. Ceci est un avantage, puisqu’il permet de détruire l’agent potentiellement pathogène du [[Team:SupBiotech-Paris/Introduction1Fr# | + | Lors de sa libération le vecteur cellulaire lyse le [[Team:SupBiotech-Paris/Concept1Fr#drapeau|vecteur tissulaire]]. Ceci est un avantage, puisqu’il permet de détruire l’agent potentiellement pathogène du [[Team:SupBiotech-Paris/Introduction1Fr#DVS|DVS]]. <br> |
Une fois libéré dans son tissu cible, le vecteur cellulaire cible les cellules d’intérêts pour y délivrer le [[Team:SupBiotech-Paris/Concept3Fr#drapeau|plasmide thérapeutique]]. <br> | Une fois libéré dans son tissu cible, le vecteur cellulaire cible les cellules d’intérêts pour y délivrer le [[Team:SupBiotech-Paris/Concept3Fr#drapeau|plasmide thérapeutique]]. <br> | ||
| + | |||
<span style="float: right">[[Team:SupBiotech-Paris/Concept2Fr#drapeau|Haut de page]]</span> | <span style="float: right">[[Team:SupBiotech-Paris/Concept2Fr#drapeau|Haut de page]]</span> | ||
| - | == Le système de ciblage cellulaire == | + | == Le système de ciblage cellulaire [1,2,9]== |
Le vecteur cellulaire a pour but de cibler les cellules d’intérêt. Pour cela, l’ajout de protéine de ciblage cellulaire, au sein du génome du bactériophage lambda, est nécessaire. | Le vecteur cellulaire a pour but de cibler les cellules d’intérêt. Pour cela, l’ajout de protéine de ciblage cellulaire, au sein du génome du bactériophage lambda, est nécessaire. | ||
La délivrance du [[Team:SupBiotech-Paris/Concept3Fr#drapeau|plasmide thérapeutique]] se fait en deux étapes : le ciblage de la cellule d’intérêt et la libération au sein du cytoplasme. | La délivrance du [[Team:SupBiotech-Paris/Concept3Fr#drapeau|plasmide thérapeutique]] se fait en deux étapes : le ciblage de la cellule d’intérêt et la libération au sein du cytoplasme. | ||
| + | |||
=== Le ciblage de la cellule d’intérêt === | === Le ciblage de la cellule d’intérêt === | ||
| - | Le bactériophage lambda interagit naturellement avec sa cellule cible, Escherichia Coli, via sa protéine de fibre de queue '''« J »'''. La protéine J étant l’unique protéine du bactériophage lambda intervenant dans la reconnaissance spécifique de la cellule hôte, elle est, par conséquent, la candidate idéale à une modification permettant de modifier le tropisme naturel du bactériophage. | + | Le bactériophage lambda interagit naturellement avec sa cellule cible, Escherichia Coli, via sa protéine de fibre de queue '''« J »'''. La protéine J étant l’unique protéine du bactériophage lambda intervenant dans la reconnaissance spécifique de la cellule hôte, elle est, par conséquent, la candidate idéale à une modification permettant de modifier le tropisme naturel du bactériophage.<br> |
Pour se faire, la protéine J est greffée à une protéine possédant la caractéristique particulière de se lier de manière spécifique à l’un des récepteurs de la cellule cible. La protéine J interagissant par le coté Cter, c’est au niveau de ce dernier qu’est placé la protéine dite de fusion.<br> | Pour se faire, la protéine J est greffée à une protéine possédant la caractéristique particulière de se lier de manière spécifique à l’un des récepteurs de la cellule cible. La protéine J interagissant par le coté Cter, c’est au niveau de ce dernier qu’est placé la protéine dite de fusion.<br> | ||
Le gène de la protéine J est donc fusionné au niveau de l’extrémité 5’ avec le gène de la [[Team:SupBiotech-Paris/BiobricksFr#drapeau| protéine de ciblage]]. La protéine qui en résulte, transcrite naturellement pendant la synthèse du vecteur cellulaire, est exprimée avec la même fréquence que la protéine native. De ce fait, lors de l’autoassemblage, le vecteur cellulaire possède la [[Team:SupBiotech-Paris/BiobricksFr#drapeau| protéine de ciblage]] sur sa queue. | Le gène de la protéine J est donc fusionné au niveau de l’extrémité 5’ avec le gène de la [[Team:SupBiotech-Paris/BiobricksFr#drapeau| protéine de ciblage]]. La protéine qui en résulte, transcrite naturellement pendant la synthèse du vecteur cellulaire, est exprimée avec la même fréquence que la protéine native. De ce fait, lors de l’autoassemblage, le vecteur cellulaire possède la [[Team:SupBiotech-Paris/BiobricksFr#drapeau| protéine de ciblage]] sur sa queue. | ||
| - | + | En fonction du type cellulaire cible, le ligand peut changer, mais l’emplacement reste le même. Le [[Team:SupBiotech-Paris/Introduction1Fr#DVS|DVS]] est par conséquent modulable à de nombreuses pathologies. | |
| - | + | ||
| - | |||
<span style="float: right">[[Team:SupBiotech-Paris/Concept2Fr#drapeau|Haut de page]]</span> | <span style="float: right">[[Team:SupBiotech-Paris/Concept2Fr#drapeau|Haut de page]]</span> | ||
| Line 98: | Line 136: | ||
Le ciblage du vecteur cellulaire est assuré par la protéine fixée sur la protéine J, en revanche pour l’internalisation et la sortie de l’endosome, la fixation à un ligand membranaire ne suffit pas. | Le ciblage du vecteur cellulaire est assuré par la protéine fixée sur la protéine J, en revanche pour l’internalisation et la sortie de l’endosome, la fixation à un ligand membranaire ne suffit pas. | ||
C’est pourquoi, le vecteur cellulaire possède une seconde protéine recombinée. Elle se trouve, cette fois-ci, sur une autre protéine, non de queue mais de tête, la '''protéine D'''. | C’est pourquoi, le vecteur cellulaire possède une seconde protéine recombinée. Elle se trouve, cette fois-ci, sur une autre protéine, non de queue mais de tête, la '''protéine D'''. | ||
| - | + | [[Image :ProteinD.png|left|frameless|150px]] | |
Le bactériophage lambda sauvage possède à sa capside, la protéine D qui est chargée de stabiliser l’ensemble de la capside, comme vu précédemment. Etant exposée sur toute la surface externe de la capside, elle est une candidate idéale pour la fusion d’une protéine d’internalisation cellulaire. | Le bactériophage lambda sauvage possède à sa capside, la protéine D qui est chargée de stabiliser l’ensemble de la capside, comme vu précédemment. Etant exposée sur toute la surface externe de la capside, elle est une candidate idéale pour la fusion d’une protéine d’internalisation cellulaire. | ||
| - | |||
La protéine D, lors de sa fixation à la capside, est organisée en trimère. Chaque monomère est distant de 5,1nm dans un trimère. La structure cristallographique de la protéine D sous sa forme trimérique montre que les extrémités, Nter et Cter, sont exposées à la surface de la capside et sont très proches les unes des autres. | La protéine D, lors de sa fixation à la capside, est organisée en trimère. Chaque monomère est distant de 5,1nm dans un trimère. La structure cristallographique de la protéine D sous sa forme trimérique montre que les extrémités, Nter et Cter, sont exposées à la surface de la capside et sont très proches les unes des autres. | ||
Les deux extrémités Nter et Cter étant exposées à la surface de la capside mature, cela laisse le choix quant au placement de la protéine de fusion. Cependant des études menées en Nter et en Cter ont montré que la fusion en Cter apportait de meilleurs résultats. | Les deux extrémités Nter et Cter étant exposées à la surface de la capside mature, cela laisse le choix quant au placement de la protéine de fusion. Cependant des études menées en Nter et en Cter ont montré que la fusion en Cter apportait de meilleurs résultats. | ||
Cette protéine d’internalisation, nommée polypeptide de type III, est issue de la base du penton des adénovirus. En plus de permettre au vecteur cellulaire d’être internalisé dans la cellule d’intérêt, elle induit sa sortir de l’endosome. | Cette protéine d’internalisation, nommée polypeptide de type III, est issue de la base du penton des adénovirus. En plus de permettre au vecteur cellulaire d’être internalisé dans la cellule d’intérêt, elle induit sa sortir de l’endosome. | ||
| - | + | [[Image :ADV5.png|center|frameless|600px]] | |
| - | + | ||
| - | [[Image :ADV5.png|center|frameless]] | + | |
| - | La base du penton est une protéine pentamérique insérée stratégiquement au niveau des douze sommets de la capside adénovirale. Son monomère d’environ 60 kDa (571 aminoacides) est présent en 60 copies dans les virus. En plus de son rôle structural dans la capside, la base du penton possède une propriété fondamentale : elle contient un motif RGD (arginine - acide aspartique - glycine) conservé, responsable de l’interaction du virus avec les intégrines αvβ3 et αvβ5. Ce motif est situé à la surface de la base du penton et se projette vers l’extérieur de la capside. | + | <div id="PB"> |
| + | La '''base du penton''' est une protéine pentamérique insérée stratégiquement au niveau des douze sommets de la capside adénovirale. Son monomère d’environ 60 kDa (571 aminoacides) est présent en 60 copies dans les virus. En plus de son rôle structural dans la capside, la base du penton possède une propriété fondamentale : elle contient un motif RGD (arginine - acide aspartique - glycine) conservé, responsable de l’interaction du virus avec les intégrines αvβ3 et αvβ5. Ce motif est situé à la surface de la base du penton et se projette vers l’extérieur de la capside. | ||
L'exposition de 5 motifs RGD portés par la base de penton (molécule pentamérique) permet l'association simultanée de plusieurs molécules d'intégrines, initiant l'entrée de l’adénovirus par endocytose, principalement au sein de vésicules à clathrines. | L'exposition de 5 motifs RGD portés par la base de penton (molécule pentamérique) permet l'association simultanée de plusieurs molécules d'intégrines, initiant l'entrée de l’adénovirus par endocytose, principalement au sein de vésicules à clathrines. | ||
| + | </div> | ||
Le phénomène d’internalisation nécessitant le regroupement des intégrines via les motifs RGD, soit plusieurs monomères de polypeptides de type III, peut soulever un problème. En effet, la protéine D n’étant fusionnée qu’à un seul monomère de polypeptide de type III, l’endocytose peut ne pas avoir lieu. | Le phénomène d’internalisation nécessitant le regroupement des intégrines via les motifs RGD, soit plusieurs monomères de polypeptides de type III, peut soulever un problème. En effet, la protéine D n’étant fusionnée qu’à un seul monomère de polypeptide de type III, l’endocytose peut ne pas avoir lieu. | ||
| Line 118: | Line 155: | ||
Le bactériophage étant naturellement infectieux pour les organismes procaryotes, l’internalisation cellulaire et la sortie de l’endosome sont des facteurs limitant pour son utilisation au sein de modèles eucaryotes. Des études ont prouvé que la base du penton améliore de manière très significative l’internalisation cellulaire et la sortie de l’endosome. | Le bactériophage étant naturellement infectieux pour les organismes procaryotes, l’internalisation cellulaire et la sortie de l’endosome sont des facteurs limitant pour son utilisation au sein de modèles eucaryotes. Des études ont prouvé que la base du penton améliore de manière très significative l’internalisation cellulaire et la sortie de l’endosome. | ||
Sans base du penton, un bactériophage perd la quasi totalité de son efficacité de transfection. C’est un élément important pour le maintien d’une bonne efficacité de transfection du vecteur cellulaire. | Sans base du penton, un bactériophage perd la quasi totalité de son efficacité de transfection. C’est un élément important pour le maintien d’une bonne efficacité de transfection du vecteur cellulaire. | ||
| - | |||
| - | |||
| - | |||
| - | |||
| - | |||
| - | |||
L’ajout de la protéine d’internalisation, le polypeptide de type III, permet au vecteur cellulaire l’internalisation et la sortie de l’endosome des cellules eucaryotes. Une fois sortie de l’endosome, le [[Team:SupBiotech-Paris/Concept3Fr#drapeau|plasmide thérapeutique]] est libéré au sein du cytoplasme de la cellule cible et peut ainsi agir. | L’ajout de la protéine d’internalisation, le polypeptide de type III, permet au vecteur cellulaire l’internalisation et la sortie de l’endosome des cellules eucaryotes. Une fois sortie de l’endosome, le [[Team:SupBiotech-Paris/Concept3Fr#drapeau|plasmide thérapeutique]] est libéré au sein du cytoplasme de la cellule cible et peut ainsi agir. | ||
| Line 131: | Line 162: | ||
== En résumé… == | == En résumé… == | ||
| - | …, le [[Team:SupBiotech-Paris/Introduction1Fr# | + | …, le [[Team:SupBiotech-Paris/Introduction1Fr#DVS|DVS]] possède un vecteur cellulaire ayant les caractéristiques suivantes : |
<div style="margin-left: 100px;"> | <div style="margin-left: 100px;"> | ||
- '''Non pathogène''' donc pas toxique, <br> | - '''Non pathogène''' donc pas toxique, <br> | ||
| Line 138: | Line 169: | ||
-'''Encapsidation et délivrance de [[Team:SupBiotech-Paris/Concept3Fr#drapeau|plasmide spécifique]]'''. <br> | -'''Encapsidation et délivrance de [[Team:SupBiotech-Paris/Concept3Fr#drapeau|plasmide spécifique]]'''. <br> | ||
</div> | </div> | ||
| - | Ces caractéristiques, spécifiques au [[Team:SupBiotech-Paris/Introduction1Fr# | + | Ces caractéristiques, spécifiques au [[Team:SupBiotech-Paris/Introduction1Fr#DVS|DVS]], apportent une solution aux problèmes récurrents, de [[Team:SupBiotech-Paris/Introduction1Fr#Spe|spécificité]] et de [[Team:SupBiotech-Paris/Introduction1Fr#PM|passage des membranes]] et de délivrance d’agent thérapeutique, rencontrés par les [[Team:SupBiotech-Paris/Introduction1Fr#drapeau|vecteurs]]. |
| + | |||
<span style="float: right">[[Team:SupBiotech-Paris/Concept2Fr#drapeau|Haut de page]]</span> | <span style="float: right">[[Team:SupBiotech-Paris/Concept2Fr#drapeau|Haut de page]]</span> | ||
| - | |||
| - | |||
| - | |||
| - | |||
Latest revision as of 00:57, 22 October 2009
Contents |
Vecteur cellulaire
Le vecteur cellulaire a pour fonction d’atteindre la cellule cible et de transfecter l’insert génique thérapeutique.
Il doit posséder certaines caractéristiques pour être un vecteur de ciblage cellulaire efficace. Il doit cibler spécifiquement le type cellulaire d’intérêt, celui à soigner. En tant que vecteur de type phagique, il doit être capable de passer la membrane de la cellule eucaryote et y délivrer son contenu de manière efficace.
Vous allez pouvoir découvrir au cours de ce chapitre sur quelles caractéristiques nous nous sommes basés pour choisir le meilleur bactériophage.
Puis, vous découvrirez plus en détails ses propriétés au travers des différentes contraintes imposées par le DVS concernant sa délivrance tissulaire, l’encapsidation du plasmide thérapeutique et le ciblage cellulaire.
Le vecteur cellulaire : Le bactériophage Lambda [1,2]
Nous avons étudié plusieurs types de bactériophages afin de sélectionner le vecteur cellulaire le plus modulable et le plus contrôlable. Pour se faire, nous avons répertorié tous les types de phages et au sein de chaque type, les espèces les mieux décrites. Plusieurs candidats ont retenu notre attention, mais c’est le bactériophage lambda qui nous a semblé le plus adapté.
Le bactériophage lambda est un virus procaryote qui infecte naturellement la bactérie Escherichia Coli. C’est un bactériophage dit tempéré, car il peut alterner phase lytique et phase lysogène sous certaines conditions. Pendant le cycle lytique, l’ADN circulaire est répliqué en grande quantité dans le cytoplasme, des progénies viraux sont formés, conduisant à la mort de la bactérie et à la libération des virions. Au cours du cycle lysogène, le génome du bactériophage est intégré dans le chromosome bactérien et est transmis à la descendance. La réplication se fait alors au rythme des divisions de la bactérie.
Naturellement infectieux pour la bactérie Escherichia Coli, le bactériophage lambda, comme tous phages, n’est pas infectieux pour l’Homme. Cette caractéristique provient du fait que leur génome est régie par des promoteurs procaryotes mais également du fait qu’ils aient une très faible capacité de transfection des cellules eucaryotes.
Enfin, l’une des caractéristiques intéressantes du bactériophage lambda est qu’il possède un ADN double brin linéaire ayant des extrémités cohésives : 12 nucléotides simple brin complémentaire, appelés séquences « Cos ». Ces extrémités cohésives ont une fonction dans l’encapsidation génomique.
L’encapsidation du plasmide thérapeutique [2,3,4,5,6,7]
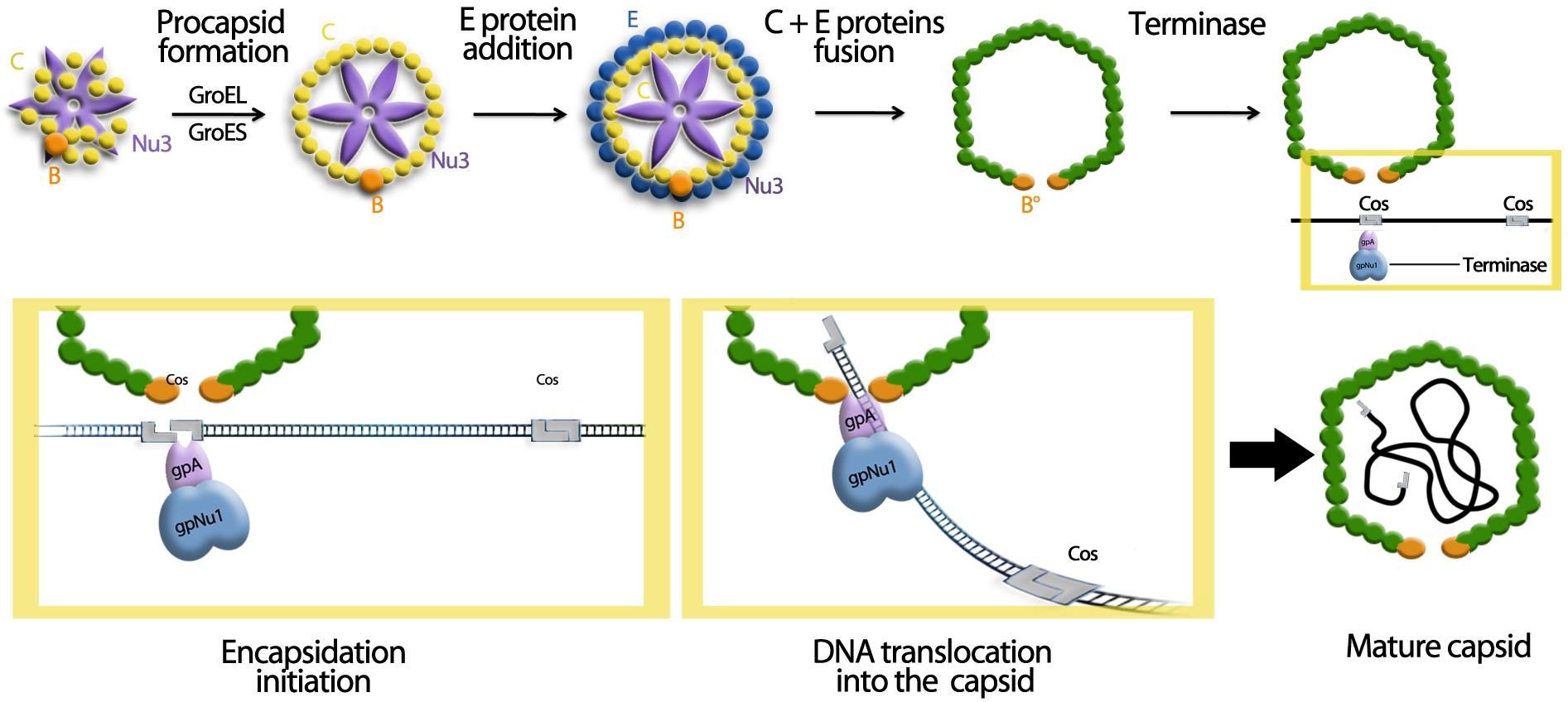
L’encapsidation du génome phagique est particulière chez le bactériophage lambda. Elle est guidée par la séquence Cos. Cette caractéristique permet l’encapsidation spécifique de séquence d’intérêt.
On observe sur le schéma ci-dessus que l’encapsidation du génome commence et se termine par les séquences Cos. Tout ce qui se trouve entre ces séquences est encapsidé. Cette particularité est utilisée en biologie moléculaire depuis de nombreuses années pour la création de banque d’ADN et d’outils moléculaires nommés Cosmides.
Nous sommes partis de ce constat pour encapsider, à l’intérieur du vecteur cellulaire, uniquement le plasmide thérapeutique. Pour se faire le génome du vecteur, le bactériophage lambda, est délété de ses séquences Cos, ces dernières sont placées sur le plasmide thérapeutique.
Séquence non codante cos : Position 1-132 et 48462-48502 : 174 paires de bases.
1.....TATCACTTTACGGGTCCTTTCCGGTGATCCGACAGGTTAC
41....GGGGCGGCGACCTCGCGGGTTTTCGCTATTTATGAAAATT
81....TTCCGGTTTAAGGCGTTTCCGTTCTTCTTCGTCATAACTT
121...AATGTTTTTATTTAAAATACCCTCTGAAAAGAAAGGAAAC
161...GACAGGTGCTGAA
Le vecteur cellulaire encapside le plasmide thérapeutique par l’intermédiaire des séquences Cos. Ainsi, il ne délivre que l’agent thérapeutique dans les cellules, ce qui permet une précaution supplémentaire au cas où le vecteur d’intérêt ne serait pas dans l’organe cible.
La délivrance du vecteur cellulaire dans l’organe cible [1,2,8]
Le vecteur cellulaire possède deux phases d’action, une phase de latence et une phase d’expression et de libération. Lors de la phase de latence, appelée cycle lysogène, le génome reste « inactif » et aucun vecteur cellulaire n’est produit au sein du vecteur tissulaire. Alors que pendant la phase d’expression et de libération, appelée cycle lytique, le génome est transcrit et répliqué, afin de produire des vecteurs cellulaires.
Cependant le vecteur tissulaire n’est pas l’hôte naturelle du vecteur cellulaire. Ainsi, si l’on veut induire une phase de latence, il nous faut la provoquer. Le système de délivrance implanté dans le vecteur tissulaire induit justement cette phase de latence.
Le plasmide de contrôle de délivrance du vecteur cellulaire induit un cycle lysogène chez ce dernier.
Le cycle lysogène est un phénomène naturellement présent chez le bactériophage lambda, le vecteur cellulaire. Lors de ce cycle, le génome phagique est inséré dans le génome bactérien sous la forme d’un prophage, il devient partie intégrante du génome de l’hôte.
A l’état de prophage, toute transcription est réprimée. Seul le gène cI, responsable du maintien du cycle lysogène, est exprimé.
La fixation de cI sur les opérateurs de la région de contrôle des promoteurs pR et pL, bloque l’expression des gènes et permet le maintien de la lysogénie. cI bloque de surcroit son propre promoteur, pRM, permettant ainsi une autorégulation de sa transcription.
Le bactériophage est maintenu sous la forme lysogène aussi longtemps que cI est exprimé. Dans le cas du DVS, l’expression de cI n’est plus contrôlée par le promoteur pRM, mais induite par un promoteur répressible LacP/O fusionné au gène cI. Si celui-ci n’est pas répressé, alors, comme dans le schéma naturel du bactériophage lambda, l’expression des gènes est inhibée.
En revanche, lorsque le signal de délivrance du vecteur cellulaire, la doxycycline, est injecté, alors le promoteur répressible LacP/O est réprimé par le répresseur LacI, synthétisé par le vecteur tissulaire.
cI inhibé, les gènes peuvent alors être transcrits, et le vecteur cellulaire synthétisé.
Système sans doxycycline:

Lors de sa libération le vecteur cellulaire lyse le vecteur tissulaire. Ceci est un avantage, puisqu’il permet de détruire l’agent potentiellement pathogène du DVS.
Une fois libéré dans son tissu cible, le vecteur cellulaire cible les cellules d’intérêts pour y délivrer le plasmide thérapeutique.
Le système de ciblage cellulaire [1,2,9]
Le vecteur cellulaire a pour but de cibler les cellules d’intérêt. Pour cela, l’ajout de protéine de ciblage cellulaire, au sein du génome du bactériophage lambda, est nécessaire. La délivrance du plasmide thérapeutique se fait en deux étapes : le ciblage de la cellule d’intérêt et la libération au sein du cytoplasme.
Le ciblage de la cellule d’intérêt
Le bactériophage lambda interagit naturellement avec sa cellule cible, Escherichia Coli, via sa protéine de fibre de queue « J ». La protéine J étant l’unique protéine du bactériophage lambda intervenant dans la reconnaissance spécifique de la cellule hôte, elle est, par conséquent, la candidate idéale à une modification permettant de modifier le tropisme naturel du bactériophage.
Pour se faire, la protéine J est greffée à une protéine possédant la caractéristique particulière de se lier de manière spécifique à l’un des récepteurs de la cellule cible. La protéine J interagissant par le coté Cter, c’est au niveau de ce dernier qu’est placé la protéine dite de fusion.
Le gène de la protéine J est donc fusionné au niveau de l’extrémité 5’ avec le gène de la protéine de ciblage. La protéine qui en résulte, transcrite naturellement pendant la synthèse du vecteur cellulaire, est exprimée avec la même fréquence que la protéine native. De ce fait, lors de l’autoassemblage, le vecteur cellulaire possède la protéine de ciblage sur sa queue.
En fonction du type cellulaire cible, le ligand peut changer, mais l’emplacement reste le même. Le DVS est par conséquent modulable à de nombreuses pathologies.
L’internalisation du vecteur cellulaire et la libération du plasmide thérapeutique
Le ciblage du vecteur cellulaire est assuré par la protéine fixée sur la protéine J, en revanche pour l’internalisation et la sortie de l’endosome, la fixation à un ligand membranaire ne suffit pas. C’est pourquoi, le vecteur cellulaire possède une seconde protéine recombinée. Elle se trouve, cette fois-ci, sur une autre protéine, non de queue mais de tête, la protéine D.
Le bactériophage lambda sauvage possède à sa capside, la protéine D qui est chargée de stabiliser l’ensemble de la capside, comme vu précédemment. Etant exposée sur toute la surface externe de la capside, elle est une candidate idéale pour la fusion d’une protéine d’internalisation cellulaire.
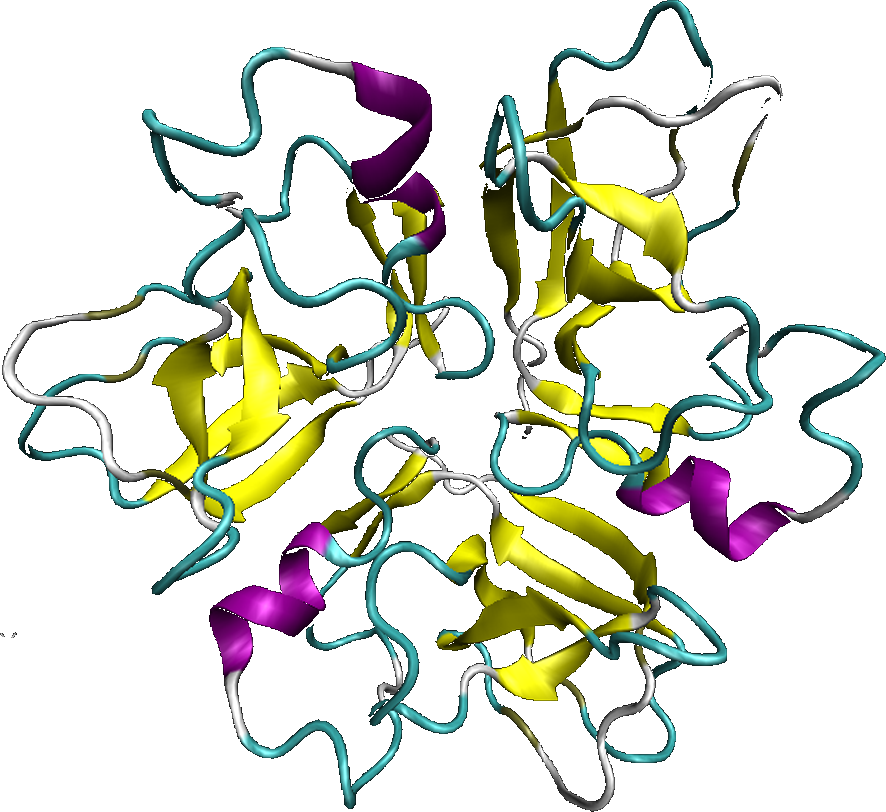
La protéine D, lors de sa fixation à la capside, est organisée en trimère. Chaque monomère est distant de 5,1nm dans un trimère. La structure cristallographique de la protéine D sous sa forme trimérique montre que les extrémités, Nter et Cter, sont exposées à la surface de la capside et sont très proches les unes des autres. Les deux extrémités Nter et Cter étant exposées à la surface de la capside mature, cela laisse le choix quant au placement de la protéine de fusion. Cependant des études menées en Nter et en Cter ont montré que la fusion en Cter apportait de meilleurs résultats. Cette protéine d’internalisation, nommée polypeptide de type III, est issue de la base du penton des adénovirus. En plus de permettre au vecteur cellulaire d’être internalisé dans la cellule d’intérêt, elle induit sa sortir de l’endosome.
La base du penton est une protéine pentamérique insérée stratégiquement au niveau des douze sommets de la capside adénovirale. Son monomère d’environ 60 kDa (571 aminoacides) est présent en 60 copies dans les virus. En plus de son rôle structural dans la capside, la base du penton possède une propriété fondamentale : elle contient un motif RGD (arginine - acide aspartique - glycine) conservé, responsable de l’interaction du virus avec les intégrines αvβ3 et αvβ5. Ce motif est situé à la surface de la base du penton et se projette vers l’extérieur de la capside. L'exposition de 5 motifs RGD portés par la base de penton (molécule pentamérique) permet l'association simultanée de plusieurs molécules d'intégrines, initiant l'entrée de l’adénovirus par endocytose, principalement au sein de vésicules à clathrines.
Le phénomène d’internalisation nécessitant le regroupement des intégrines via les motifs RGD, soit plusieurs monomères de polypeptides de type III, peut soulever un problème. En effet, la protéine D n’étant fusionnée qu’à un seul monomère de polypeptide de type III, l’endocytose peut ne pas avoir lieu. Cependant, d’après une étude cristallographique, la distance entre deux motifs RGD sur une base du penton est de 5,7nm. La distance entre deux protéines D étant similaire (5,1nm), le regroupement des intégrines peut avoir lieu et induire l’internalisation et la sortie de l’endosome.
Le bactériophage étant naturellement infectieux pour les organismes procaryotes, l’internalisation cellulaire et la sortie de l’endosome sont des facteurs limitant pour son utilisation au sein de modèles eucaryotes. Des études ont prouvé que la base du penton améliore de manière très significative l’internalisation cellulaire et la sortie de l’endosome. Sans base du penton, un bactériophage perd la quasi totalité de son efficacité de transfection. C’est un élément important pour le maintien d’une bonne efficacité de transfection du vecteur cellulaire.
L’ajout de la protéine d’internalisation, le polypeptide de type III, permet au vecteur cellulaire l’internalisation et la sortie de l’endosome des cellules eucaryotes. Une fois sortie de l’endosome, le plasmide thérapeutique est libéré au sein du cytoplasme de la cellule cible et peut ainsi agir.
En résumé…
…, le DVS possède un vecteur cellulaire ayant les caractéristiques suivantes :
- Non pathogène donc pas toxique,
- Ciblage cellulaire, donc 2nde spécificité
- Passage des membranes des cellules eucaryotes,
-Encapsidation et délivrance de plasmide spécifique.
Ces caractéristiques, spécifiques au DVS, apportent une solution aux problèmes récurrents, de spécificité et de passage des membranes et de délivrance d’agent thérapeutique, rencontrés par les vecteurs.
 "
"