Team:SupBiotech-Paris/Ciblage Tissulaire
From 2009.igem.org
(→Conclusion) |
(→Détails du protocole expérimental) |
||
| (One intermediate revision not shown) | |||
| Line 33: | Line 33: | ||
=== Détails du protocole expérimental === | === Détails du protocole expérimental === | ||
| - | :*Jour -7 : Inoculation de 10^ | + | :*Jour -7 : Inoculation de 4.10^6 cellules LPB (cellules cancéreuses fibroblastiques) en sous-cutanée, sur 2 souris blacks.<br> |
:*Jour 0 : Inoculation de 10^6 CFU.ml-1* de vecteurs tissulaires, <i>M. avium</i>, en IV (intraveineuse) par la queue, sur les 3 modèles murins : Immunodéprimé, cancéreux, et normal (2 souris par modèle). | :*Jour 0 : Inoculation de 10^6 CFU.ml-1* de vecteurs tissulaires, <i>M. avium</i>, en IV (intraveineuse) par la queue, sur les 3 modèles murins : Immunodéprimé, cancéreux, et normal (2 souris par modèle). | ||
::La concentration de vecteurs tissulaires à injecter, a été déterminée par mesure de la densité optique. La densité optique d’une concentration à 10^6 bactéries n’est pas détectable au spectrophotomètre. Nous avons donc mesuré l’absorbance d’une suspension cellulaire à 10^8 bactéries. Une fois, dilué par 100, celle-ci a la concentration souhaitée soit : 10^6 bactéries.<br> | ::La concentration de vecteurs tissulaires à injecter, a été déterminée par mesure de la densité optique. La densité optique d’une concentration à 10^6 bactéries n’est pas détectable au spectrophotomètre. Nous avons donc mesuré l’absorbance d’une suspension cellulaire à 10^8 bactéries. Une fois, dilué par 100, celle-ci a la concentration souhaitée soit : 10^6 bactéries.<br> | ||
| Line 78: | Line 78: | ||
Bien que notre étude ne prouve pas significativement la présence de <i>M. avium</i> dans le poumon, il a été prouvé mainte fois que ce type de bactérie colonise le poumon. Cet organe est l'un des tropismes naturels de ''M. avium'' chez la souris, comme chez l’homme.<br> | Bien que notre étude ne prouve pas significativement la présence de <i>M. avium</i> dans le poumon, il a été prouvé mainte fois que ce type de bactérie colonise le poumon. Cet organe est l'un des tropismes naturels de ''M. avium'' chez la souris, comme chez l’homme.<br> | ||
| - | Le [[Team:SupBiotech-Paris/Introduction1Fr#DVS|DVS]]peut donc être utilisé sur le cancer du poumon, car nous avons la certitude que le [[Team:SupBiotech-Paris/Concept1Fr#drapeau|vecteur tissulaire]] peut cibler l'organe et y libérer le [[Team:SupBiotech-Paris/Concept2Fr#Drapeau|vecteur cellulaire]].<br> | + | Le [[Team:SupBiotech-Paris/Introduction1Fr#DVS|DVS]] peut donc être utilisé sur le cancer du poumon, car nous avons la certitude que le [[Team:SupBiotech-Paris/Concept1Fr#drapeau|vecteur tissulaire]] peut cibler l'organe et y libérer le [[Team:SupBiotech-Paris/Concept2Fr#Drapeau|vecteur cellulaire]].<br> |
Latest revision as of 01:03, 21 October 2009
Contents |
Ciblage tissulaire
Contexte
Le cancer du poumon non à petite cellules, ou NSCLC, est un cancer ayant une zone de développement à la lumière de l’organe. Cette localisation tumorale est essentiellement du aux facteurs déclenchant la tumorogénèse (exemple : Tabac). Une voie d’accès logique pour l’administration du traitement, serait la voie aérosol, par nébulisation de la bactérie. Mais, cette voie n’est pas celle que nous avons choisie pour notre traitement. Le traitement DVS appliqué au cancer du poumon est administré en intraveineuse.
Objectif
Nous avons décidé de vérifier et de quantifier la présence de Mycobactérium avium, le vecteur tissulaire, au sein du poumon, lors d’une administration en intraveineuse. Pour cela, nous avons réalisé une étude in vivo dans plusieurs modèles murins.
Démarche expérimentale
Dans le cadre de cette étude in vivo, nous avons conçu un protocole de bioluminescence, qui permet de suivre en temps réel, la propagation de notre vecteur tissulaire dans les souris. La bioluminescence est un bon système rapporteur pour analyser l'implantation des mycobactéries et la clairance in vivo. Nous avons utilisé un outil qui nous a été aimablement fournie par le Dr Brian D. Robertson (chercheur de l'Imperial College London). Cet outils est un plasmide qui va être électroporé dans M. avium, M. avium va alors pouvoir produire la firefly luciférase, gène rapporteur, permettant le suivi. En effet, la luciférase en catalysant l'oxydation de la luciférine en oxyluciferine, va entrainer une émission de photons qui peut-être capté par une caméra CCD photosensible (IVIS, Imaging System 50, Xenogen).
Malheureusement, la croissance des mycobactéries électroporées avec le plasmide de suivi, a été bien trop lente pour pouvoir réaliser cette étude dans les temps impartis (Pour rappel, temps de génération de M. avium: environ 20 heures). Nous avons donc décidé de changer notre protocole.
Suite à ce manque de temps, nous avons utilisé un autre protocole afin de vérifier et quantifier la présence de notre vecteur tissulaire dans le poumon. Nous avons décidé d’injecter M. avium wild type et une semaine après l’injection d’observer sa présence dans les organes, par prélèvement tissulaire. Pour cela, nous avons étudié la littérature afin de déterminer quelle dose de M. avium pouvait être injectée dans un modèle murin. Différentes études, sur diverses pathologies d’origines bactériennes, faisait état de l’injection par voie intraveineuse d’une concentration de bactéries de 105 à 107 CFU.ml-1 (colony forming units) par souris.
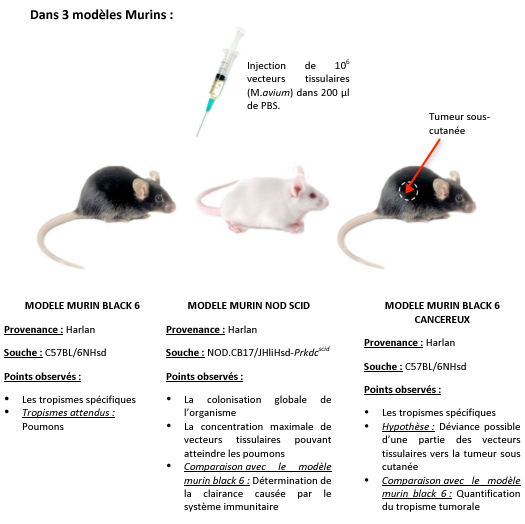
Nous avons choisis de réaliser cette expérience sur 3 modèles murins : Immunodéprimé, normal et cancéreux.
D’après certaines études, ils sembleraient, que les mycobactéries est une affinité particulière pour les fibronectines, surexprimées à la surface des cellules tumorales. Aucun tropisme mycobactérien pour une zone tumorale n’a pour l’instant été démontré, ce dernier modèle murin nous permet ainsi de vérifier cette hypothèse.
Détails du protocole expérimental
- Jour -7 : Inoculation de 4.10^6 cellules LPB (cellules cancéreuses fibroblastiques) en sous-cutanée, sur 2 souris blacks.
- Jour 0 : Inoculation de 10^6 CFU.ml-1* de vecteurs tissulaires, M. avium, en IV (intraveineuse) par la queue, sur les 3 modèles murins : Immunodéprimé, cancéreux, et normal (2 souris par modèle).
- La concentration de vecteurs tissulaires à injecter, a été déterminée par mesure de la densité optique. La densité optique d’une concentration à 10^6 bactéries n’est pas détectable au spectrophotomètre. Nous avons donc mesuré l’absorbance d’une suspension cellulaire à 10^8 bactéries. Une fois, dilué par 100, celle-ci a la concentration souhaitée soit : 10^6 bactéries.
- Jour -7 : Inoculation de 4.10^6 cellules LPB (cellules cancéreuses fibroblastiques) en sous-cutanée, sur 2 souris blacks.
- Jour 7 : Sacrifice des souris, Extraction des organes et obtention d’une suspension cellulaire, à partir des poumons, du foie, de la rate.
- Jour 7 : Sacrifice des souris, Extraction des organes et obtention d’une suspension cellulaire, à partir des poumons, du foie, de la rate.
La suspension cellulaire obtenue est diluée puis analysée par cytométrie en flux (5.10^5 évènements seront comptabilisés par le cytomètre), pour vérifier la taille et la granulosité des cellules. Ces 2 caractéristiques sont totalement différentes entre les cellules eucaryotes qui composent les organes murins, et le vecteur tissulaire, M. avium d’origine procaryote.
On peut ainsi vérifier et quantifier la présence du vecteur tissulaire.
Résultats
Un échantillon pulmonaire de chacun des modèles murins, a été analysé par cytomètrie en flux, afin de déterminer et de quantifier la présence de notre vecteur tissulaire, M. avium dans les poumons. Cette expérience n’ayant pu être répété plus d’une fois, nous ne pouvons qu’être réservé par rapport à ces résultats brutes. Néanmoins différentes publications ont déjà prouvé une implantation de Mycobactérium aviumau sein des poumons, prouvant ainsi la crédibilité et la faisabilité de l’étude.
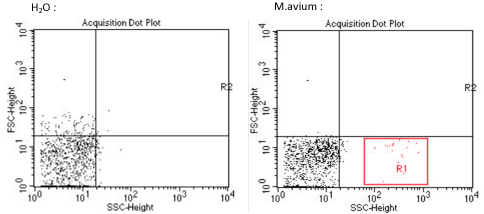
D’après les résultats ci-dessus, nous avons déterminé la signature d’un échantillon de Mycobacterium avium en cytométrie en flux (en rouge zone R1). L’image de gauche correspond au bruit de fond ou signaux parasites du cytomètre. Il aurait été cependant très intéressant de réaliser un 3e témoin, avec l’acquisition d’un échantillon de poumons de souris non infecté par M. avium.
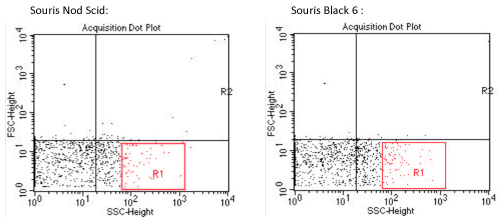
Dans les échantillons ci-dessus, il est difficile de retrouver spécifiquement, la signature de l’échantillon de Mycobacterium. Il est aussi très difficile de distinguer une quelconque différence entre les 2 modèle murins, Nod Scid et Black 6.
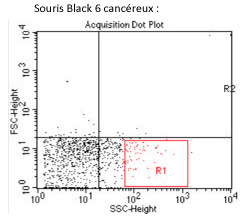
L’échantillons ci-contre, ne nous permet pas de déterminer une éventuelle influence d’une tumeur sous-cutanée, sur le tropisme mycobactérien, ni même de différencier le tropisme de M. avium dans ce modèle, de ceux des autres modèles.
Discussion
Cette expérience réalisée une unique fois, n’a pas permis de répondre à nos objectifs, afin de déterminer et quantifier les tropismes de M. avium. Cependant, le manque de temps est aussi un facteur à prendre en considération. En effet, cette analyse par cytométrie en flux n’a été réalisée qu’une semaine après l’injection de M. avium dans les souris. A la lecture de différentes publications, il est intéressant de noter que les données significatives de l’implantation de M. avium dans les poumons, sont obtenues qu’après de nombreuses semaines. D’où, sans doute notre difficulté à quantifier par cytométrie, la présence du vecteur tissulaire après une semaine.
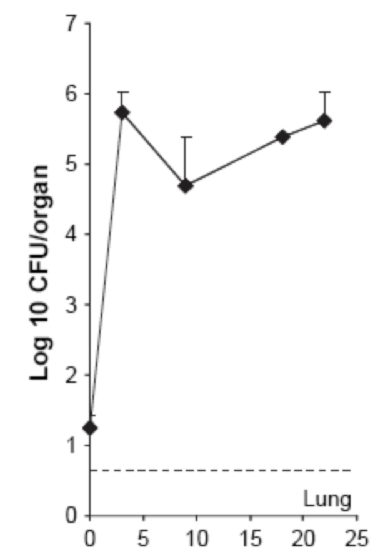
La figure ci-dessus est tiré de la publication « Thymus as a target for mycobacterial infections ». Le même type de protocole a été réalisé, avec injection de 10^6 CFU/ml de M. avium administré par voie intraveineuse. Il est décrit dans cette figure que les poumons sont infectés dès le premier jour de l’infection, mais en très petite quantité (légèrement supérieur à 10^1, puis de manière prolongée avec une propagation rapide (de 10^1 à 10^6 CFU/organe en moins de 5 semaines). Ceci prouve donc bien que les poumons sont colonisé par M. avium.
Conclusion
Bien que notre étude ne prouve pas significativement la présence de M. avium dans le poumon, il a été prouvé mainte fois que ce type de bactérie colonise le poumon. Cet organe est l'un des tropismes naturels de M. avium chez la souris, comme chez l’homme.
Le DVS peut donc être utilisé sur le cancer du poumon, car nous avons la certitude que le vecteur tissulaire peut cibler l'organe et y libérer le vecteur cellulaire.
 "
"