Team:SupBiotech-Paris/Concept1Fr
From 2009.igem.org
Enguerrand (Talk | contribs) (→Système de délivrance du vecteur cellulaire) |
Enguerrand (Talk | contribs) (→Système de délivrance du vecteur cellulaire) |
||
| Line 123: | Line 123: | ||
- un [[Team:SupBiotech-Paris/BiobricksFr#drapeau|opérateur LacP/O]] implanté dans le génome du [[Team:SupBiotech-Paris/Concept2Fr#drapeau|vecteur cellulaire]] et contrôlant l’expression de ses gènes via le contrôle de l’expression du répresseur phagique.<br> | - un [[Team:SupBiotech-Paris/BiobricksFr#drapeau|opérateur LacP/O]] implanté dans le génome du [[Team:SupBiotech-Paris/Concept2Fr#drapeau|vecteur cellulaire]] et contrôlant l’expression de ses gènes via le contrôle de l’expression du répresseur phagique.<br> | ||
[[Image :controledelysogenie2.png|frameless|caption|left|300px]] | [[Image :controledelysogenie2.png|frameless|caption|left|300px]] | ||
| - | |||
| - | |||
Revision as of 23:21, 21 October 2009
Contents |
Le vecteur tissulaire
Le vecteur tissulaire a pour fonction de véhiculer le vecteur cellulaire jusqu'à l’organe d’intérêt, celui comportant la cellule cible.
Il doit posséder trois caractéristiques essentielles. En tant que vecteur de type bactérien, il ne doit pas être pathogène pour le patient, ou du moins peut être peu néfaste. Il doit avoir un tropisme intéressant, c'est-à-dire avoir la capacité d’atteindre l’organe cible. Et enfin, la caractéristique la plus importante, il doit pouvoir déjouer le système immunitaire, afin de ne pas être détruit ou éliminé avant d’avoir atteint ses objectifs.
Vous allez découvrir au cours de ce chapitre sur quelles caractéristiques nous nous sommes basées pour choisir la meilleure bactérie.
Puis, vous découvrirez plus en détails ses propriétés au travers des différentes contraintes imposées par le DVS concernant sa pathogénicité, sa résistance et son tropisme.
Enfin, nous vous présenterons une amélioration apportée à la bactérie pour en faire un vecteur tissulaire optimal.
Le vecteur tissulaire : Mycobacterium avium [1,2]
Nous avons étudié plusieurs types bactériens pour déterminer le meilleur rapport entre une faible pathogénicité, un tropisme intéressant et une bonne résistance au système immunitaire, afin de choisir au mieux le vecteur tissulaire.
Une tâche ardue, puisqu’en règle générale, un microorganisme qui résiste au système immunitaire est potentiellement dangereux pour son hôte. Il fallait donc trouver un microorganisme résistant mais ne possédant pas une haute pathogénicité pour l’Homme. Etant plus facile de réduire la pathogénicité que d’améliorer la résistance, nous avons déterminé ce dernier facteur comme prioritaire pour la sélection.
Nous avons tout d’abord répertorié les bactéries présentant une résistance au système immunitaire. Les quatre plus connues étant :
- Mycobacterium tuberculosis, agent responsable de la tuberculose;
- Legionella pneumophila, agent responsable de la légionellose;
- Listeria monocytogenes, agent responsable de la méningite;
- Coxiella burnetii, agent responsable de la coxiellose (fièvre Q).
Toutes les quatre sont bien évidemment hautement pathogènes, nous nous sommes donc penchés sur leurs homologues ou sous-espèces peu pathogènes pour l’homme.
Mycobacterium avium (M.avium) est la bactérie qui a retenu notre attention. Cette dernière appartient au genre des Mycobactéries, et plus précisément au Complexe Mycobacterium Avium (MAC).
M.avium est nettement moins pathogène que son homologue Mycobacterium tuberculosis. Les seules manifestations cliniques qu’elle peut induire sont: toux productive, fatigue, fièvre, perte de poids et sueurs nocturnes. Ces symptômes découlent de la colonisation du tractus respiratoire ou gastro-intestinal et de la diffusion possible à d'autres endroits du corps. Les M.avium sont peu pathogènes; c'est pourquoi elles peuvent coloniser des sujets sans avoir d'effets indésirables sur leur santé. Les sujets immunocompétents qui n'ont pas de maladie sous-jacente ont un très faible risque de présenter des symptômes d'infection par M.avium. Des rapports épidémiologiques ont récemment montré que l'on retrouve de plus en plus la présence de M.avium chez des sujets, notamment des femmes, qui ne semblent avoir aucun trouble pulmonaire ou immunitaire prédisposant. La majorité des sujets en bonne santé qui sont atteints d'infections causées par des M.avium ont une infection localisée; par contre, on constate des infections par M.avium disséminées chez un pourcentage important de patients atteints du SIDA (80 % des patients colonisés), ainsi que chez d'autres populations dont le système immunitaire est déficient, comme les sujets qui ont un syndrôme d'immunodéficience combinée aiguë ou qui ont reçu une transplantation et chez les patients traités aux corticostéroïdes ou avec des médicaments cytotoxiques.
M.avium semble être un candidat des plus intéressants pour le vecteur tissulaire. Cette bactérie résiste au système immunitaire et est peu pathogène pour l’Homme.
Résistance au système immunitaire du vecteur tissulaire [3,4,5]
Le système immunitaire peut s’avérer être un ennemi redoutable, détectant et éliminant tout ce qui n’appartient pas à l’organisme. Ne pouvant être furtif à ce dernier, il faut être « blindé ».
Pour cela le vecteur tissulaire possède deux atouts, un système de détournement du système immunitaire et une paroi robuste.
Mécanisme de détournement du système immunitaire
Les bactéries comme Mycobacterium avium ont développé des stratégies de résistance hautement spécifiques pour déjouer le système immunitaire.
Ainsi M.avium, microorganisme intracellulaire facultatif, possède la capacité d’infecter certaines cellules du système immunitaire que sont les macrophages ou les cellules dendritiques, responsables de la phagocytose.
L’infection engendrant la mort de ces phagocytes, on observe chez l’hôte une diminution de son immunité non spécifique, ce qui permet à M.avium de persister chez son hôte.
Afin de lutter contre les macrophages, M.avium inhibe la maturation des phagolysosomes, initialement responsable de la lyse des bactéries. Le paradigme de ce mécanisme n’est pas encore déterminé, mais l’hypothèse principale implique l’un des glycolipides de la paroi, le lipoarabinomannan.
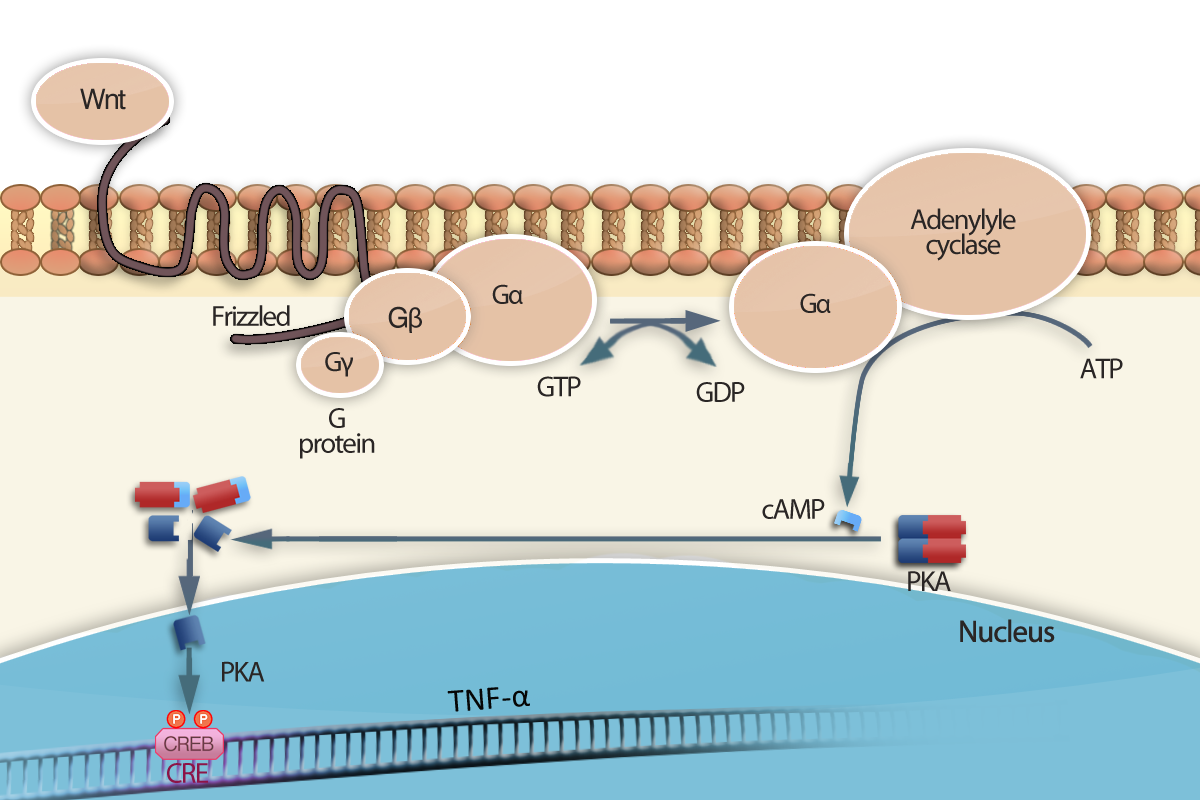
Pour lutter contre les cellules dendritiques, M.avium dérègle les signaux de transduction cellulaire en libérant certaines enzymes régulant le taux de messagers secondaires.
En effet, M.avium possède, dans son génome, 12 gènes contenant des domaines d’adenylate cyclases de classes III, dont la plus importante est Rv0386. Celle-ci facilite la formation d’AMPc dans les macrophages. L’AMPc est un messager secondaire qui mène à la synthèse de cytokines pro-inflammatoires TNF-a
Or, on sait qu’à forte concentration, le TNF-a bloque la maturation des cellules dendritiques et donc le déclenchement de la réponse immunitaire.
M.avium ne « craignant rien » face au système immunitaire son élimination est faible. Elle a alors la capacité de persister dans l’organisme et donc plus de chance d’atteindre sa cible et de s’y implanter.
Paroi cellulaire et enveloppe du vecteur tissulaire
La capacité de Mycobacterium à résister au système immunitaire est essentiellement dû à sa paroi et son enveloppe cellulaire. Ces dernières présentent une structure complexe et spécifique aux Mycobactéries.
Véritable cuirasse, l’enveloppe de M.avium est composée de nombreux éléments. Certains, comme les protéines solubles, les carbohydrates, et les lipides sont communs à toutes les bactéries.
- le peptidoglycane,
- l’acide mycolique.
Ensemble, ces 3 constituants forment le cœur mycoylarabinogalactanpeptidoglycane (MAGP) de la paroi cellulaire. Le MAGP représente un des deux lipopolysaccharides (LPS) commun à toutes les mycobactéries, mais M.avium possède un second LPS : le lipoarabinomannan.
On observe également, chez M.avium, une couche de glycopeptidolipides (GPL) tout aussi spécifique.
Toute cette structure (MAGP, GPL et lipoarabinomannan) est fortement immunogène tout comme l’est le LPS des autres bactéries. Mais contrairement aux autres bactéries, cette structure complexe confère, à M.avium, une résistance spéciale. Le réseau formé par la membrane, basé sur des hydrocarbonés parallèles, rend la mycobactérie imperméable à de nombreux agents comme l’éthanol, les détergents ou les antibiotiques classiques.
La paroi du vecteur tissulaire et sa faculté à synthétiser des perturbateurs de transduction cellulaire lui permettent d’être l’un des seuls vecteurs résistants au système immunitaire. Ceci étant surement l’un des atouts majeur du DVS.
Les tissus cibles du DVS [6,7]
Le DVS peut s’attaquer à plusieurs physiopathologies en fonction des tropismes de son vecteur tissulaire. Ces derniers sont évidemment liés à ceux de M.avium « Wild-type », mais il est envisageable de transformer M.avium pour la rendre sensible à certains chimiotactismes organiques. Pour l’heure, découvrons ce que permet M.avium « Wild-type ».
M.avium peut infecter un organisme par voie orale et par voie sanguine. Si son homologue, M.tuberculosis est souvent vu comme un agent pathogène pulmonaire, les M.avium peuvent potentiellement infecter tous les organes. Cette affirmation est vérifiée chez les patients immunodéprimés au sein desquels la diminution de l’immunité permet à la mycobactérie de se propager dans l’organisme entier.
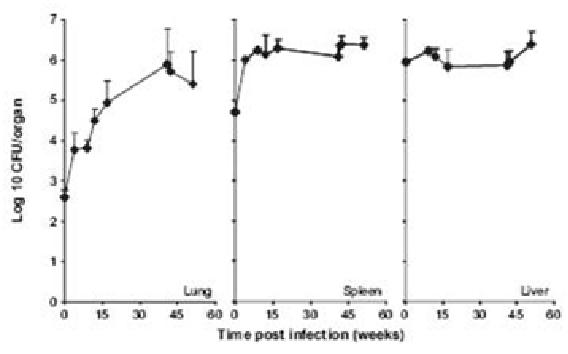
Des recherches plus poussées sur le tropisme tissulaire ont révélé certains organes cibles. Il est montré que quelques semaines après l’infection, la concentration de bactérie atteint un plateau dans deux organes : le foie et la rate puis plus tard dans un troisième : les poumons.
Figure 2: Invasion des poumons, de la rate, du foie et du thymus par M.avium de 0 à 52 semaines en log de 10 (6 à 10 souris)
On observe également que, durant de nombreuses semaines post-infection, la charge bactérienne continue à augmenter. Or, cette augmentation dans les tissus cibles n’est pas corrélée avec une augmentation de Mycobacterium dans le sang. Cette augmentation est donc le fruit d’une invasion des tissus cibles et non d’une invasion du corps dans son intégralité.
Il y a donc un tropisme mais également une implantation du vecteur dans les tissus cibles. Cette caractéristique est très intéressante car le vecteur n’est pas circulant mais résident.
Le vecteur tissulaire possède donc trois tropismes intéressants et identifiés. Le DVS offre ainsi une application thérapeutique sur des physiopathologies touchant les poumons, la rate et le foie.
Il peut les cibler, s’y implanter, et s’y développer jusqu’à recevoir le signal de délivrance du vecteur cellulaire.
Système de délivrance du vecteur cellulaire
Le vecteur tissulaire a pour fonction première de délivrer le vecteur cellulaire dans l’organe cible. Si la libération se fait trop tôt, le vecteur cellulaire n’a que peu de chance d’atteindre sa cellule d’intérêt. Seul, le vecteur cellulaire est éliminé par l’organisme, mais au sein du vecteur tissulaire, il est en sécurité.
Un système implanté dans la bactérie permet de contrôler l’expression et donc la libération du vecteur cellulaire.
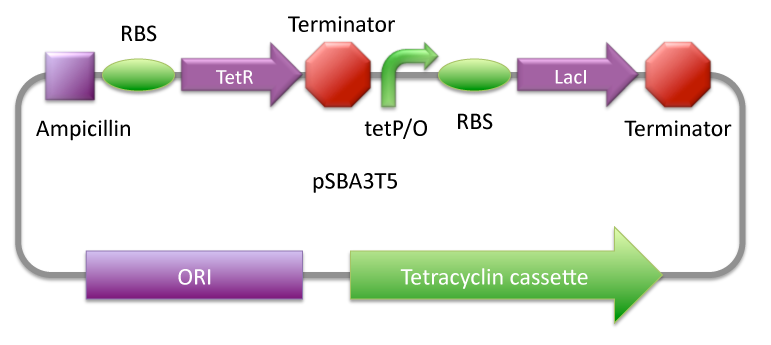
Ce système de contrôle par la doxycycline, implanté dans le vecteur tissulaire est fait de deux éléments :
- un plasmide de synthèse de LacI, contrôlé par la doxycycline.
Ce premier plasmide code pour le répresseur LacI sous le contrôle du promoteur répressé (pTET). L’activité de pTET, et donc l’expression de LacI, dépend entièrement de la fixation de doxycycline sur le répresseur TetR.
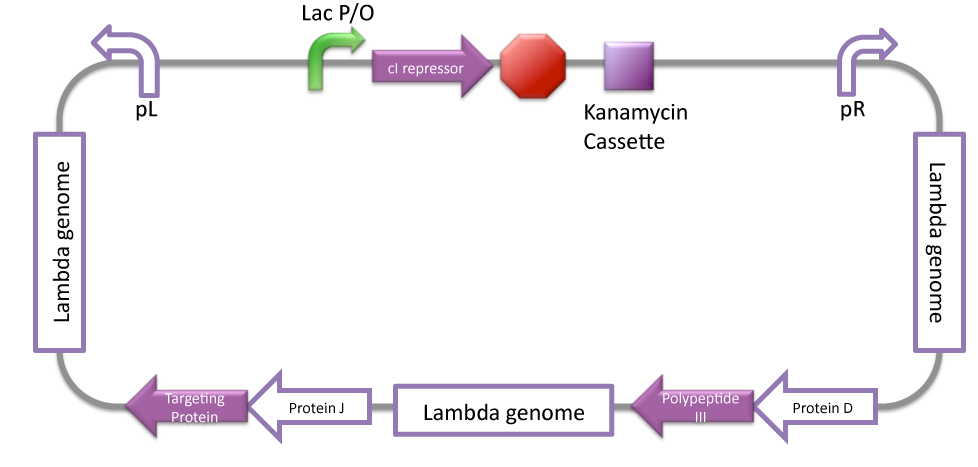
- un opérateur LacP/O implanté dans le génome du vecteur cellulaire et contrôlant l’expression de ses gènes via le contrôle de l’expression du répresseur phagique.
Lac I se fixe sur le promoteur LacP/O du génome phagique inhibant l’expression de son répresseur..
La répression de l’expression du vecteur cellulaire est faite de manière constante par un répresseur phagique. En présence de doxycycline, l’expression du répresseur phagique est inhibée promouvant l’expression du vecteur cellulaire.
Le système de délivrance permet le maintien du vecteur cellulaire à l’intérieur du vecteur tissulaire sous le contrôle de la doxycycline. Le suivi de la M.avium et la mise en place de moyen statistique pour déterminer la cinétique de propagation sont essentiels. Ces informations permettent de déterminer les temps d’injection. L’injection de doxycycline déclenche la libération du vecteur cellulaire qui lyse le vecteur tissulaire et diffuse dans l’organe cible.
En résumé…
…, le DVS possède un vecteur tissulaire ayant les caractéristiques suivantes :
- Faible pathogénicité donc faible toxicité,
- Résistance au système immunitaire et donc faible clairance,
- Ciblage tissulaire donc première spécificité,
- Synthèse de délivrance du vecteur cellulaire.
Ces caractéristiques, spécifiques au DVS, apportent une solution aux problèmes récurrents, de spécificité et d’élimination par le système immunitaire, rencontrés par les vecteurs.
 "
"