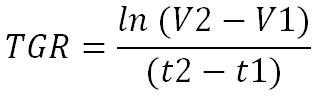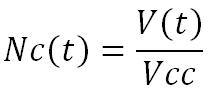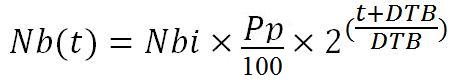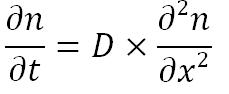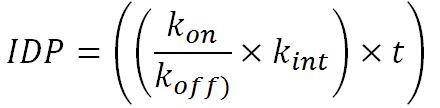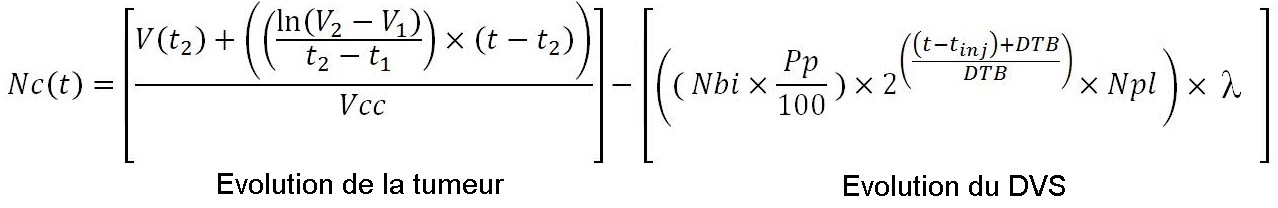Team:SupBiotech-Paris/Modeling du traitement
From 2009.igem.org
Contexte
Le cancer du poumon non à petites cellules, ou NSCLC, est un cancer dit agressif, avec une vitesse de développement relativement forte. Les traitements sont souvent inefficaces, car le développement de la tumeur est plus rapide que son élimination par les médicaments.
Objectif
Nous avons décidé de modéliser l’efficacité de notre traitement face à ce type de tumeur. Pour cela, nous avons modélisé l’évolution de la tumeur, l’évolution de notre traitement et son efficacité.
L’objectif de la modélisation est de vérifier si notre traitement est capable d’éliminer la tumeur dans son intégralité.
Segmentation du modèle
Pour commencer il a fallu retracer le schéma d’action complet du DVS et l’évolution de la tumeur. Ensuite, dans chaque étape du traitement, il a fallu identifier tous les paramètres qui entrent en jeu et analyser leurs actions, les uns par rapport aux autres, afin de déterminer les équations du modèle.
Pour simplifier l’équation, tout en dressant un modèle réaliste, il nous a fallu découper chaque étape et les modéliser séparément.
Première étape : le développement de la tumeur en fonction du temps
On considère la tumeur non métastasique et sa croissance exponentielle.
Soit une tumeur de volume V1 en cm3 à un instant t1.
Soit la même tumeur, à un instant t2, avec un volume V2.
La tumeur est considérée en phase de croissance exponentielle et sans métastase donc l’équation qui régit son développement, le Tumor Growth Rate (TGR), est égale à :
Ainsi, le Volume de la tumeur (Vc), à un instant t, est égal à :
Enfin, connaissant le volume moyen d’une cellule cancéreuse, valeur obtenu expérimentalement, on peut déterminer, si l’on considère la tumeur comme pleine, c'est-à-dire sans cavité ou vaisseau sanguin, que le Nombre de cellule cancéreuse en fonction du temps (Nc(t)), sans action du traitement, est égal à :
Avec Vcc le volume d’une cellule cancéreuse.
Deuxième étape : Le développement du vecteur tissulaire
Le vecteur tissulaire est injecté au patient à un temps t, proche de t2. Le Nombre de vecteurs injectés (Nbi) est de 1x10^6. Le tropisme pulmonaire du vecteur n’est pas parfait, seul un Pourcentage (Pp) va au poumon. Le nombre total de vecteurs tissulaires dans le corps augmente, car ce vecteur est de type bactérien et possède donc un Temps de Doublement (DTB).
On peut ainsi établir que le Nombre de vecteurs tissulaires dans les poumons est égal à :
Le nombre de vecteurs tissulaires augmente jusqu’à l’injection de la doxycycline, où dès lors ces derniers sont lysés pour libérer les vecteurs cellulaires dans le poumon.
Ce temps d’injection n’est pas anodin. En effet, si l’on attend suffisamment longtemps, le nombre de vecteurs tissulaires est suffisant pour éliminer la tumeur ou du moins la réduire de façon importante.
On peut ainsi se servir de la modélisation pour déterminer le Temps optimal d’Injection de la doxycyline (Tinj).
Troisième étape : La libération du vecteur cellulaire
Une fois la doxycycline injectée, le vecteur cellulaire est libéré. Le nombre de vecteurs cellulaires est proportionnel au nombre de vecteurs tissulaires dans le poumon. Or, on sait que la valeur moyenne de Phage recombinant libéré par M. avium (Npl) est de 100.
On peut écrire que le Nombre de vecteurs cellulaires au moment de l’injection (Np(Tinj)) est égal à :
Le nombre de vecteurs cellulaires ne croit pas comme pour le vecteur tissulaire. En effet, il décroit au fur et à mesure du temps, pour cause la stabilité et internalisation cellulaire (pour libérer le plasmide thérapeutique).
Sa stabilité sanguine est égale à la Constante de Dégradation du phage (kdeg), ainsi, si l’on implémente cette dégradation dans l’équation de Np(t) on obtient la formule suivante :
L’étape de dispersion du phage dans la tumeur et celle d’internalisation cellulaire, en vue de leur complexité, représente des étapes à elles seules.
Quatrième étape : La dispersion du vecteur cellulaire
On considère, pour notre modèle, que le sang est un fluide newtonien avec une vitesse Vmax fixe au cours du temps. On néglige les à-coups cardiaques et les flux turbulents liés aux cavités de l’épithélium sanguin.
Le vecteur cellulaire se déplace selon deux axes. Un axe X dans le sens du flux sanguin et un axe Y, orthogonal à l’axe X.
Le déplacement en Y est dépendant de la diffusion du phage dans le sang. Le déplacement en Y dépend de l’équation de diffusion d’une particule dans un fluide.
Avec n, le nombre de particule, et D, le coefficient de diffusion.
Le déplacement en X dépend uniquement de la propagation du flux sanguin dans le vaisseau. On néglige la diffusion en X, 1000 fois inférieure à la propagation du flux sanguin. Les phages se déplacent à différentes vitesses réparties de façon parabolique, allant de Vmax au centre du vaisseau à V0 sur la paroi du vaisseau.
On peut donc déterminer en combien de temps la particule de vitesse Vmax, c'est-à-dire la particule la plus loin de la paroi du vaisseau, atteint le bord. On obtient le temps nécessaire à l’internalisation de tous les phages d’une bactérie.
Couplé au déplacement en X, c'est-à-dire à la vitesse du flux sanguin, et intégré sur le périmetre d’un vaisseau sanguin, on obtient la surface d’action des vecteur cellulaire issu d’un vecteur tissulaire. Par cette équation on sait combien de cellules cancéreuses sont détruit pour 100 vecteur cellulaire ou 1 vecteur Tissulaire
La vitesse de diffusion du vecteur cellulaire D est égale à 0,5µm.s-1 or la taille d’un capillaire sanguin est de 10µm de diamètre. La particule la plus éloignée met donc 10s à toucher une paroi du vaisseau.
Grâce à ce temps et connaissant la vitesse du flux sanguin dans les capillaires, soit 1x10^3µm.s-1, on peut déterminer que les vecteur cellulaire libérés par un vecteur tissulaire couvrent une zone de 1x10^4µm de longueur (L), pour 10µm de diamètre (2r), soit une surface égale à 2π x L x r., égale à 31,4x10^4µm².
Ainsi, un vecteur tissulaire peut potentiellement cibler plus de 31 000 cellules cancéreuses, or, il ne possède que 100 vecteur cellulaire. On peut simplifier l’équation en disant que 100 vecteur cellulaire détruisent 100 cellules cancéreuse et donc réduire l’équation de dispersion à une constante.
Une fois chaque phage ayant atteint la paroi, entre en jeu l’internalisation dont le modèle répond à deux schéma d’action.
Cinquième étape : L’internalisation du vecteur cellulaire
Une fois au contact de la cellule, le vecteur cellulaire a deux schémas d’action. Le premier schéma, le vecteur se fixe puis il se détache de la cellule. Le second schéma, le vecteur se fixe puis il se fait internaliser au sein de la cellule.
On peut modéliser cela en fonction du temps et des Constantes d’Association (kon) , de Dissociation (koff) et d’Internalisation (kint) .
Les étapes les plus courtes, en échelle de temps, sont certainement les étapes concernant le phage. L’internalisation est la plus courte d’entre elle, selon les constantes plus de 320 vecteurs cellulaires sont internalisés par seconde au contact d’une paroi.
On peut ainsi réduire cette équation en fonction du temps à une simple constante.
Une fois internalisé, le plasmide thérapeutique engendre l’apoptose de la cellule en 1h, diminuant le nombre de cellule cancéreuse, Nc(t), et le volume tumoral, Vc.
Equation finale du modèle
L’équation finale de notre modèle en fonction du temps est égale à :
Avec :
- Nc(t), le nombre de cellules cancéreuses dans le temps,
- V(t), le volume tumoral,
- V1 et V2, deux volumes tumoraux à respectivement des temps t1 et t2,
- Vcc, le volume d’une cellule cancéreuse,
- Nbi, le nombre de vecteurs tissulaire injectés,
- Pp, le pourcentage pulmonaire de vecteurs tissulaires par rapport à la dose injectée,
- DTB, le temps de doublement du vecteur tissulaire,
- Npl, le nombre de vecteurs cellulaires libérés par bactérie.
On peut négliger, en vue des différences d’échelles de temps ou d’espace, certains facteurs :
- Kdeg, la constante de dégradation du phage, car tous les phages sont internalisés en 10s.
- D, la diffusion du phage et IDP, l’internalisation cellulaire, car on considère que 100 phages rentrent dans 100 cellules différentes (pour une valeur potentielle de 31400) donc tout cela est égal à 1.
Simulation de traitement
MATLAB !
 "
"